Глюкозо- и неглюкозоиндуцированная митохондриальная дисфункция при диабетической болезни почек
Jan 17, 2024
Абстрактный:Митохондриальная дисфункцияиграет важную роль в патогенезе и прогрессированиидиабетическая болезнь почек(ДКД). В этом обзоре мы обсудим митохондриальную дисфункцию, наблюдаемую удоклинические модели ДКДа также в клинической ДКД с акцентом наокислительного фосфорилирования(OXPHOS), митохондриальныеактивные формы кислорода(mtROS), биогенез, деление и слияние, митофагия и митохондриальные биомаркеры мочи. Будут обсуждаться как глюкозо-, так и неглюкозо-индуцированные митохондриальные дисфункции. Что касается митохондриальной дисфункции, вызванной глюкозой, происходит энергетический сдвиг от OXPHOS к аэробному гликолизу, называемый эффектом Варбурга, и образующиеся в результате токсичные промежуточные продукты метаболизма глюкозы способствуютТравма, вызванная ДКД. Что касается митохондриальной дисфункции, не вызванной глюкозой, мы рассмотрим роль липотоксичности, гипоксии и вазоактивных путей, включая сигнальные пути эндотелина-1 (Edn1)/Edn1 рецептора типа А. Хотя относительный вклад каждого из этих путей в ДБП остается неясным, цель этого обзора — подчеркнуть сложностьмитохондриальная дисфункцияв ДКД и обсудить, как маркеры митохондриальной дисфункции могут помочь нам стратифицироватьпациенты с риском развития ДБП.
Ключевые слова: диабетическая болезнь почек; митохондриальная дисфункция;митохондриальные активные формы кислорода; Эффект Варбурга

НАЖМИТЕ ЗДЕСЬ, ЧТОБЫ ПОЛУЧИТЬ НАТУРАЛЬНЫЙ ОРГАНИЧЕСКИЙ ЭКСТРАКТ ЦИСТАНШИ С 25% ЭХИНАКОЗИДА И 9% АКТЕОЗИДА ДЛЯ ФУНКЦИИ ПОЧЕК
1. Введение
Растет число больных сахарным диабетом.диабетическая болезнь почек(ДКД) является важной причинойдиабетический микрососудистыйосложнений, что является независимым фактором риска смертности и сердечно-сосудистых событий [1].
Почки являются одним из наиболее энергозатратных органов и после сердца занимают второе место по экспрессии белков, участвующих в функции митохондрий и потреблении кислорода [2,3]. Почки требуют энергии главным образом для реабсорбции растворенных веществ, среди других задач, включая удаление отходов, поддержание электролитного и жидкостного баланса, а также кислотно-щелочного гомеостаза [4]. Генерация ионного градиента через плазматическую мембрану с помощью Na+/K+ -АТФазы необходима для реабсорбции растворенных веществ. Таким образом, предполагается, что митохондриальная дисфункция играет центральную роль в патогенезе и прогрессировании заболеваний почек, включая ДБП [5–7].
Поскольку каждый компонент нефрона играет различную роль и имеет разные энергетические потребности, причины и фенотипы митохондриальной дисфункции могут различаться в зависимости от типа клеток в почках. В этом обзоре мы обсудим связанные с глюкозой и несвязанные пути митохондриальной дисфункции, способствующие ДБП, с точки зрения категорий, а также причин.

2. Митохондриальная дисфункция при ДБП.
Из-за решающей роли митохондрий как электростанции клеток, митохондриальная дисфункция традиционно относится к изменению выработки аденозинтрифосфата (АТФ) путем окислительного фосфорилирования (OXPHOS). Однако по мере расширения нашего понимания различных ролей, которые играют митохондрии, митохондриальная дисфункция теперь включает в себя любые аномальные биологические процессы в митохондриях [7]. В этом разделе мы обсудим различные категории митохондриальной дисфункции, возникающей при ДБП, и обсудим их потенциальную причинную роль (рис. 1).
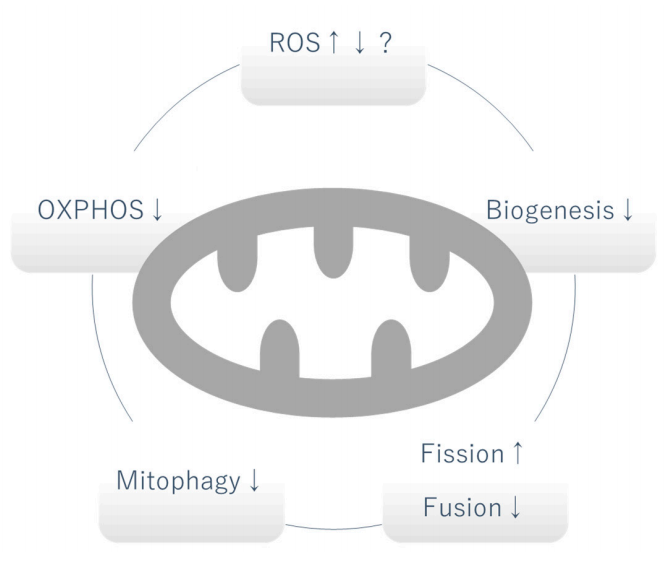
Рисунок 1. Митохондриальная дисфункция при ДБП. Вопрос о повышении или понижении уровня митохондриальных АФК является спорным и может варьироваться в зависимости от стадии ДБП. OXPHOS, митофагия и биогенез обычно снижены. Повышенное деление и пониженное слияние вызывают фрагментацию митохондрий. OXPHOS: окислительное фосфорилирование, ROS: активные формы кислорода, f: увеличено.: уменьшено.
2.1. Митохондриальное окислительное фосфорилирование (OXPHOS)
Центральная роль митохондрий как электростанции клеток заключается в выработке аденозинтрифосфата (АТФ). Метаболиты глюкозы, липидов и аминокислот транспортируются в митохондриальный матрикс, служащие субстратами цикла трикарбоновых кислот (ICA). NADH и FADH2 генерируются вместе с реакционными электронами, подающими электроны в Комплексы I и II электрон-транспортной цепи (ETC). . По мере переноса электронов ионы H+ перекачиваются в межмембранное пространство. Комплекс V или АТФ-синтазы использует этот протонный градиент для генерации АТФ (рис. 2). Показатели активности и приспособленности OXPHOS включают скорость потребления кислорода (OCR), продукцию АТФ, мембранный потенциал и оценку каждого комплекса (активность, образование). В целом наблюдалось, что OCR в корковом веществе почек увеличивается на ранней стадии ДБП с последующим снижением по мере прогрессирования ДБП, тогда как в клубочках и подоцитах OCR снижается как на ранней, так и на поздней фазе заболевания [5]. Хотя существуют некоторые несоответствия между результатами исследований и активностью комплекса, было показано, что они снижаются, по крайней мере, на поздней стадии ДБП (8,9). Вклад снижения активации OXPHOS в ДБП можно сделать из наблюдения, что некоторые генетические мутации в OXPHOS , такие как однонуклеотидные полиморфизмы (SNP) в коферменте 05 (CO05) и цитохромоксидазе (COX6A1), связаны с DKD у людей (101. CO05 кодирует метилтрансферазу, локализованную в митохондриальном матриксе, а COX6A1 кодирует субъединицу цитохрома c, который часть ЕТК.
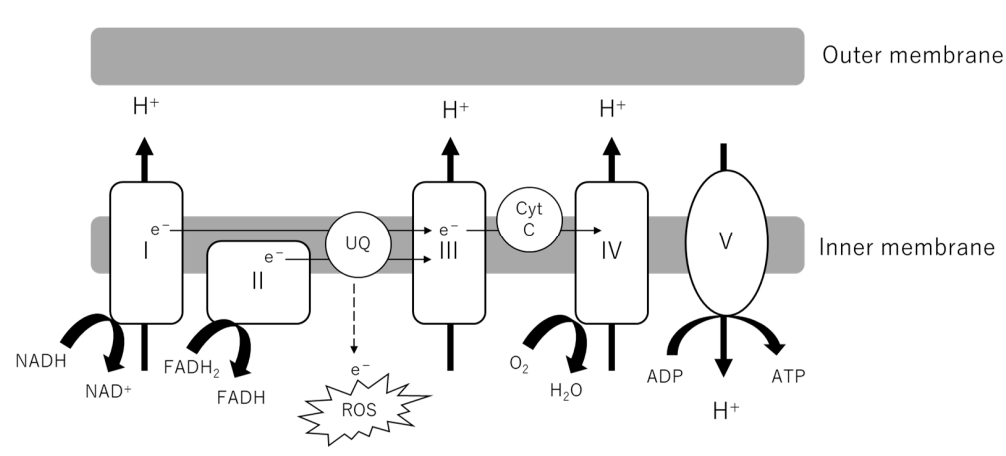
Рисунок 2. Электронно-транспортная цепь (ЭТС) во внутренней мембране митохондрий. НАДН и ФАДН2 из цикла ТСА отдают электроны Комплексам I и II. Когда электроны транспортируются через ETC, генерируется протонный градиент, который Комплекс V или АТФ-синтаза соединяется с синтезом АТФ. Утечка электронов из ETC вызывает образование АФК. АДФ, аденозиндифосфат; АТФ, аденозинтрифосфат; Cyt C, цитохромный комплекс; АФК – активные формы кислорода; UQ, убихинон; Цикл ТСА, цикл трикарбоновых кислот.
2.2. Митохондриальные активные формы кислорода (mtROS)
С тех пор, как Браунли и его коллеги в 2000 году предположили, что индуцированные гипергликемией митохондриальные активные формы кислорода (мтАФК) являются объединяющим механизмом микрососудистых осложнений диабета, эта парадигма стала преобладать [11,12]. В последнее время источник АФК при ДБП и патогенная роль АФК стали спорными [13,14]. Хотя может быть достигнут консенсус в отношении того, что повреждение, вызванное АФК, увеличивается при ДБП, существуют противоречивые исследования относительно изменений в выработке мтАФК, которые можно объяснить различными методами, используемыми для обнаружения мтАФК, или различными моделями или временными точками ДБП. Как в живых, так и в фиксированных почках мышей db/db повышенное содержание АФК в митохондриях наблюдалось с использованием зонда зеленого флуоресцентного белка, локализованного в митохондриальном матриксе и чувствительного к восстановлению-окислению [15]. Напротив, у мышей C57BL/6J, которым вводили стрептозотоцин (STZ), и мышей Ins2- Akita (мыши DBA/B6 F1) наблюдалось снижение митохондриального супероксида при системном введении дигидроэтидия (DHE) как в живых, так и в фиксированных почках. [16]. Последнее исследование не исключает выработку АФК в других клеточных компартментах, включая эндоплазматический ретикулум (ЭР) или ферментные системы, такие как никотинамидадениндинуклеотидфосфатоксидаза (Nox). Примечательно, что восстановление митохондриального биогенеза и активности OX PHOS за счет активации аденозинмонофосфат-активируемой протеинкиназы (AMPK) увеличивало mtROS и улучшало фенотип DKD, что свидетельствует против роли mtROS в стимулировании DKD.
АФК не играют исключительно вредной роли в клеточной биологии. Митохондриальный гормезис — это концепция, согласно которой незначительное усиление митохондриального супероксида на исходном уровне может снизить восприимчивость к более тяжелому клеточному стрессу [13]. АФК также играют важную роль в некоторых сигнальных путях клеток, что требует дальнейшего выяснения сложных характеристик АФК.

2.3. Биогенез
Клетки справляются с растущей потребностью в энергии за счет увеличения биогенеза митохондрий, при котором функциональные митохондрии генерируются путем дупликации митохондриальной ДНК (мтДНК) и последующего бинарного деления. Коактиватор 1 рецептора, активируемого пролифератором пероксисом (PGC1), играет центральную роль в митохондриальном биогенезе [17]. PGC1 является регулятором транскрипции митохондриальных метаболических путей, таких как окислительное фосфорилирование (OXPHOS), цикл ТСА и метаболизм жирных кислот. Рецепторы, активирующие пролифератор пероксисом PGC1 (PPAR), и эстроген-связанные рецепторы (ERR) также могут служить коактиваторами PGC1. PGC1 димеризуется с коактиваторами транскрипции для регуляции последующей транскрипции генов, и эти партнеры включают циклический AMP-чувствительный элемент-связывающий белок (CREB), ядерные респираторные факторы 1 и 2 (NRF1 и NRF2) и активированные PPAR и ERR [4]. Пути, чувствительные к питательным веществам, такие как механическая мишень рапамицина (mTOR), AMPK, сиртуин, циклический АМФ (цАМФ) и циклический гуанозинмонофосфат (цГМФ), регулируют PGC1 прямо или косвенно.
При ДБП, хотя существуют некоторые расхождения между исследованиями, возможно, из-за анализа на разных стадиях заболевания, считается, что активность PGC1 увеличивается на ранней стадии диабета, как показано на мышах db/db 8-недельного возраста, с последующим снижением активности на более поздних стадиях, как было продемонстрировано у пациентов перед трансплантацией и у мышей через 24 недели после индукции диабета инъекцией СТЗ [8,16,18,19]. Ген 1, активирующий таурин (Tug1), длинный некодирующий ген, был описан как регулятор PGC1 в подоцитах при ДБП [20]. Было продемонстрировано, что Tug1 связывается с элементом, расположенным выше Ppargc1a, и взаимодействует с PGC1, связывающимся с его собственным промотором, впоследствии усиливая активность промотора Ppargc1a.
2.4. Митохондриальное деление и слияние
Митохондрии — это динамические органеллы, в которых происходят строго контролируемые процессы деления и слияния. Деление митохондрий опосредовано динамин-1-подобным белком (DRP1) и его рецепторами, такими как фактор деления 1 (FIS1), фактор деления митохондрий (MFF) и белки митохондриальной динамики массой 49 и 51 кДа (MID49 и MID51). Слияние митохондрий опосредуется длинными изоформами белка атрофии зрительного нерва 1 (OPA1), который играет роль в слиянии внутренней митохондриальной мембраны, и митофузинами (MFN1 и MFN2), которые играют роль в слиянии внешней митохондриальной мембраны [5,6].
Хотя увеличение факторов деления и слияния митохондрий, таких как длинные изоформы OPA1, MFN1, MFN2 и MFF, наблюдалось на ранней стадии ДБП, у крыс, которым инъецировали STZ, митохондрии последовательно фрагментировались на ранних и поздних стадиях [8]. Биопсия почек человека у пациентов с ДБП также выявила фрагментированные митохондрии в подоцитах и клетках проксимальных канальцев [21,22]. В соответствии с усилением деления и снижением слияния, экспрессия Drp1 и FIS1 была увеличена, в то время как в последнем исследовании было показано, что экспрессия MFN2 снижена в канальцах.
2.5. Митофагия
Аутофагия — это путь, который разлагает и перерабатывает поврежденные органеллы и макромолекулы, а селективная аутофагия митохондрий называется митофагией. Митофагия играет решающую роль в поддержании качества митохондрий путем удаления поврежденных митохондрий. Митофагия может быть опосредована предполагаемой киназой 1 (PINK1)/паркин-опосредованным путем, индуцированной фосфатазой и гомологом тензина, и другими белками внешней митохондриальной мембраны, такими как белок 3 BCL2/аденовируса E1B 19 кДа (BNIP3) и NIP{{10 }}подобно белку X (NIX) или белку 1, содержащему домен FUN14 рецептора митофагии (FUNDC1).
Пути, опосредованные PINK1 и паркином, изучены более тщательно, чем другие [23]. PINK1 имеет киназный домен Ser/Thr и встроен как во внутреннюю, так и во внешнюю митохондриальную мембрану. В здоровых митохондриях PINK1 расщепляется в двух точках митохондриальными протеазами, что приводит к его диссоциации от митохондриальной мембраны и деградации системой убиквитин-протеасома. В деполяризованных митохондриях PINK1 избегает расщепления и стабильно находится на внешней мембране. Впоследствии PINK1 гомодимеризуется и аутофосфорилируется, рекрутируя E3 убиквитинлигазу паркин и убиквитин, направляя митохондрии на путь митофагии. В убиквитин-независимом пути белки внешней митохондриальной мембраны, такие как BNIP3, NIX или FUNDC1, рекрутируют ассоциированный с микротрубочками белок 1A/1B легкой цепи 3 (LC3) и индуцируют митофагию при определенных стимулах, включая гипоксию [24,25]. Кардиолипин, который в норме находится во внутренней мембране митохондрий, при определенных стимулах экстернализируется и обнаруживается с помощью LC3, способствуя поглощению митохондрий аутофагосомами [26]. P62 является маркером аутофагического груза, и его накопление может указывать на застой в деградации через аутофагический поток. В целом уровень базальной митофагии подоцитов высок, что можно объяснить их терминально дифференцированными характеристиками. Напротив, в трубчатых клетках исходный уровень митофагии низок, но он может индуцироваться вследствие стресса.
Митофагия подавляется при ДБП, о чем свидетельствуют низкие уровни экспрессии PINK1/паркина в подоцитах STZ-индуцированных мышей с диабетом и повышенные уровни экспрессии р62 в тубулярных клетках биопсии, полученных от пациентов с ДБП [27–29]. Белок, взаимодействующий с тиоредоксином (TXNIP), участвует в подавлении тубулярной аутофагии и митофагии, индуцированной высоким содержанием глюкозы [27]. Было также показано, что высокий уровень глюкозы ингибирует транскрипционную активность класса O1 forkhead-box (FoxO1) посредством его фосфорилирования с помощью Akt (протеинкиназа B), что приводит к снижению регуляции PINK1 [29]. Защитный эффект митохинона на ДКД частично объясняется восстановлением экспрессии белков PINK1 и паркина в тубулярных клетках посредством активации NRF2 [30].
2.6. Мочевой митохондриальный биомаркер
Важно надежно выявить ДБП на ранней стадии заболевания, предпочтительно до того, как станет очевидной микроальбуминурия или снижение расчетной скорости клубочковой фильтрации (рСКФ), чтобы предотвратить дальнейшее прогрессирование до терминальной стадии заболевания почек. Поскольку считается, что митохондриальная дисфункция предшествует явным гистологическим изменениям при ДБП, в последнее время активно исследуются биомаркеры митохондриальной дисфункции. Несмотря на то, что в этих исследованиях изучались пациенты с установленной ДБП, они могут быть полезны для выявления биомаркеров у пациентов, страдающих ДБП. Исследование метаболитов в моче выявило глобальное подавление митохондриального дыхания у пациентов с ДБП по сравнению с контрольной группой без ДБП [19]. В соответствии с представлением о том, что мтДНК высвобождается из поврежденных клеток канальцев, то же исследование продемонстрировало увеличение количества мтДНК в моче. Хотя мтДНК мочи имела умеренную, но значимую обратную корреляцию с внутрипочечной мтДНК и рСКФ на исходном уровне, была обнаружена положительная корреляция с интерстициальным фиброзом. МтДНК мочи или мтДНК биоптатов существенно не коррелировали со снижением рСКФ в течение 24 месяцев наблюдения [31]. Необходимы дальнейшие исследования, чтобы определить, можно ли использовать митохондриальные биомаркеры в клинической практике.
Служба поддержки Wecistanche-крупнейшего экспортера цистаншей в Китае:
Электронная почта:wallence.suen@wecistanche.com
Whatsapp/Телефон:+86 15292862950
Магазин для получения дополнительных технических характеристик:
https://www.xjcistanche.com/cistanche-shop







