Улучшение терапевтической вакцинации против гепатита В — выводы из доклинических моделей иммунотерапии против персистирующей вирусной инфекции гепатита В, часть 2
Jun 28, 2023
Комбинация факторов влияет на иммунный ответ на инфекцию ВГВ, образование вирусспецифических эффекторных Т-клеток и элиминацию инфицированных ВГВ гепатоцитов. Стоит отметить, что клиренс HBV у естественного хозяина, то есть у шимпанзе, требует нескольких месяцев [61,62], что отличается от иммунного ответа на другие вирусы, такие как грипп, нацеленные на легочную ткань, где наблюдаются быстрые иммунные ответы [63]. .
Эта потребность в течение длительного периода для удаления инфицированных гепатоцитов из печени не только после инфицирования ВГВ, но и после инфицирования ВГА или ВГС указывает на особые препятствия, которые необходимо преодолеть иммунному ответу хозяина, чтобы установить вирусспецифический иммунитет и элиминировать вирус. -инфицированные гепатоциты.
3. Стратегии лечебной вакцинации против хронического гепатита В
Для создания терапевтической вакцины против хронического гепатита В использовались различные подходы. Чаще всего они основывались на новых знаниях об иммунопатогенезе инфекции ВГВ и новых технологиях для повышения силы вирусспецифического иммунитета. Однако одной из основных проблем при разработке иммунотерапии против хронического гепатита В является отсутствие подходящей животной модели, которая точно отражает все особенности инфекции ВГВ у людей [64]. HBV человека имеет строгие видовые ограничения. Только шимпанзе восприимчивы к инфекции HBV, и важные открытия были сделаны в отношении инфекционности HBV и противовирусных иммунных реакций в этой модели [4,62,65] до того, как исследование было остановлено по этическим причинам.
Заражение вирусом гепатита В может привести к длительной хронической стимуляции иммунной системы организма, что может привести к иммунным нарушениям и иммуносупрессии. Вирус размножается в печени и высвобождает большое количество вирусных частиц, которые активируют иммунные клетки, такие как Т-клетки, макрофаги и дендритные клетки, вызывая воспалительную реакцию. В то же время вирус также может подавлять активность иммунных клеток, что делает иммунные клетки неспособными эффективно уничтожать вирус.
По мере увеличения времени заражения иммунная система организма постепенно теряет способность контролировать вирус гепатита В, что приводит к размножению большого количества возбудителей в организме. В это время в организме появляются некоторые иммунные аномалии, такие как снижение уровня антител и уменьшение количества CD4 плюс Т-лимфоцитов. Все это приведет к снижению иммунитета организма, и легко заразиться другими болезнетворными микроорганизмами, такими как бактерии и вирусы, которые осложнят течение болезни.
Поэтому поддержание достаточного и хорошего иммунитета является одним из важных средств профилактики и контроля за инфекцией, вызванной вирусом гепатита В. Усиление физических упражнений, поддержание хорошего психического состояния, формирование хороших жизненных привычек и обеспечение достаточного сна могут улучшить иммунитет организма. В то же время своевременная вакцинация против гепатита В, улучшение личной гигиены и недопущение ненужных половых контактов также могут эффективно предотвратить заражение вирусом гепатита В. Поэтому надо повышать иммунитет. Цистанхе обладает эффектом значительного повышения иммунитета. Полисахариды в мясе могут регулировать иммунный ответ иммунной системы человека, улучшать стрессоустойчивость иммунных клеток и усиливать бактерицидный эффект иммунных клеток.

Нажмите Польза цистанхе для здоровья
Хотя существуют модели заражения отдельных видов животных их специфическими вирусами гепатита В, такими как, например, вирус гепатита В уток и уток (DHBV) и вирус гепатита В сурков и сурков (WHBV), эти модели ограничены важными различиями. между вирусами и HBV человека, с несовместимостью антигена, а также с заметными различиями в иммунных реакциях и отсутствием инструментов для изучения вирусспецифического иммунитета. Мыши, как предпочтительные доклинические животные модели для изучения иммунного патогенеза, также используются для изучения патогенеза ВГВ.
Однако для доставки HBV в гепатоциты видов, инфицирование которых невозможно, были разработаны различные стратегии: во-первых, генетическая манипуляция (трансгенные мыши, экспрессирующие геном HBV); во-вторых, гидродинамическая инъекция геномов HBV или, в-третьих, вирусные носители для доставки геномов HBV в гепатоциты [66,67]. Таким образом, большая часть наших знаний об иммунопатогенезе персистирующей инфекции HBV и экспериментальных подходах, направленных на конкретные иммунные механизмы контроля персистирующей инфекции, была получена на неоптимальных моделях инфекции HBV.
Многочисленные клинические испытания были проведены у пациентов с хроническим гепатитом В, чтобы изучить важность конкретных концепций восстановления защитного иммунитета после установления персистирующей инфекции ВГВ [68–70]. В профилактических вакцинах упор делается на индукцию иммунитета против поверхностных антигенов HBV, чтобы вызвать нейтрализующие анти-HB антитела и предотвратить инфекцию. Индукция HBs-специфических CD8 T-клеток, которые нацеливаются на HBsAg-экспрессирующие инфицированные гепатоциты и уничтожают их, менее важна.
Напротив, при терапевтической вакцинации другие вирусные антигены, в частности, ядерный антиген HB и вирусная полимераза, нацелены на увеличение широты вирус-специфического ответа эффекторных Т-клеток, и основное внимание уделяется индукции мощных Т-клеток CD4 и CD8. ответы. В целом, все стратегии разработки терапевтической вакцинации против хронического гепатита В включали снижение репликации вируса.
Далее мы рассмотрим различные стратегии, используемые для разработки терапевтической вакцинации против хронического гепатита В, и их результаты.
4. Усиление иммуногенности вакцинации против хронического гепатита В.
Концептуальная идея стратегии терапевтической вакцинации заключается в предположении, что недостаточная индукция HBV-специфического В- и Т-клеточного иммунитета является причиной отсутствия элиминации вируса [69,71–73].
Были предприняты многочисленные подходы для повышения иммуногенности вакцин против хронического гепатита В и, таким образом, создания сильного вирусспецифического иммунитета против поверхностных, нуклеокапсидных или полимеразных антигенов ВГВ, который затем должен контролировать инфекцию ВГВ путем индукции вирусспецифических нейтрализующих антител и элиминация инфицированных вирусом гепатоцитов через эффекторные Т-клетки. Первые попытки наладить терапевтическую вакцинацию больных хроническим гепатитом В были предприняты путем увеличения количества введений вакцин, которые изначально разрабатывались для использования в качестве профилактических вакцин и, следовательно, нацелены на HBsAg.
Большинство вакцин содержат квасцы в качестве адъюванта, который, как было показано, вызывает индукцию врожденного иммунитета через все еще довольно плохо определенные пути [74] и вызывает сильное смещение Th2. В попытке повысить иммуногенность профилактические вакцины вводили в разные места и, в частности, внутрикожно, поскольку локальная внутрикожная активация иммунных ответов считается более эффективной [75]. Кроме того, вакцины, нацеленные на Т-клетки, или комбинации HBsAg и HBcAg в качестве иммуногенов исследовались на предмет их эффективности при терапевтической вакцинации [76–78]. Однако все эти подходы не привели к излечению пациентов с хроническим гепатитом В [59,70,71].
Ключом к успеху профилактических рекомбинантных вакцин является использование адъювантов [74], которые являются основой для передачи сигнала 3 антигенпрезентирующим клеткам и индукции локального воспаления и, следовательно, должным образом запускают Т-клеточный иммунитет. Таким образом, квасцы, индуцируя сильное смещение Th2, предотвращают индукцию ответов эффекторных Т-клеток. Использование других адъювантов в сочетании с антигенами HBV в виде частиц показало многообещающие результаты, по крайней мере, в доклинических моделях [79]. Открытие лигандов для иммунных сенсорных молекул, таких как лиганды для TLR7, TLR8, TLR9 и циклического ди-АМФ в качестве лиганда для пути cGAS/STING, а также лиганды для цитозольного рецептора распознавания РНК RIG-I или МДА-5 вызвали значительный интерес к их терапевтическому применению при хроническом гепатите В.
Адъюванты служат для запуска воспаления и, более конкретно, функционального созревания дендритных клеток, тем самым увеличивая силу иммунного ответа против рекомбинантных антигенов. Например, TLR9 экспрессируется на профессиональных антигенпрезентирующих В- и дендритных клетках, поэтому лиганды TLR9, используемые в качестве адъюванта, могут оказывать положительное влияние на иммуногенность против антигенов, включенных в вакцину [74,80]. Недавно на рынок была выпущена новая профилактическая вакцина против гепатита В, включающая лиганд TLR9- в качестве адъюванта, демонстрирующая превосходство над вакцинами на основе квасцов [81]. Будет интересно посмотреть, продемонстрирует ли он эффективность в терапевтических условиях против хронического гепатита В.

Учитывая постоянное воздействие на персистентно инфицированного хозяина антигенов HBV, в частности высоких уровней циркулирующего HBsAg, было высказано предположение, что применение адъювантов может быть достаточным для запуска HBV-специфического иммунитета [74]. В соответствии с этим пероральная доставка лигандов TLR, которая, как считается, ведет через портальный венозный дренаж кишечника к доставке лигандов TLR в печень, оценивалась как вариант лечения хронического гепатита В [82,83]. Кроме того, было показано, что лиганды для цитозольных иммунных сенсорных рецепторов, таких как геликаза RIG-I, эффективны в борьбе с экспериментальной инфекцией HBV [84–86]. В клинических испытаниях до сих пор не было достигнуто ни контроля над HBV, ни излечения от хронического гепатита B с помощью агонистов TLR, что указывает на то, что применение агонистов TLR может не приводить к индукции HBV-специфического иммунитета, а только запуск врожденного иммунитета и воспаления может недостаточно для преодоления иммунной толерантности и достижения контроля над хроническим гепатитом В. Однако альтернативные агонисты рецепторов распознавания образов, запускающие TLR8, Rig-I или STING, в настоящее время проходят клинические испытания; будет интересно посмотреть на результат.
Выбор иммуногена в вакцине также имеет ключевое значение. В то время как профилактические вакцины должны индуцировать только нейтрализующие антитела, направленные против белков оболочки HBV, терапевтические вакцины, скорее всего, должны индуцировать широкий Т-клеточный ответ и, следовательно, должны включать другие антигены HBV, такие как ядро HBV и полимераза [70]. Интересный подход идентифицировал белок HBV X как ценную мишень для вакцинации с использованием доклинической модели персистирующей инфекции HBV [87]. Белок HBV X экспрессируется на гораздо более низких уровнях, чем другие вирусные белки, и его низкое содержание в инфицированной печени может стать лучшей мишенью для вакцинации, поскольку высокие уровни экспрессии антигена модельных вирусов часто связаны с развитием Т-клеточного истощения [88]. ]. Однако гепатоциты с их низким уровнем экспрессии MHC-I также могут не презентировать какой-либо пептид из этого небольшого X-белка.
Еще одним подходом к повышению иммуногенности вакцин при хроническом гепатите В является разработка стратегий гетерологичной первичной бустерной вакцинации [70]. Комбинации адъювантных белковых вакцин, вакцинации ДНК и векторной иммунизации были протестированы на различных доклинических моделях персистирующих инфекций ВГВ и дали многообещающие результаты [89–91]. Концептуально разработка вакцин с использованием вирусных векторов для доставки антигенов HBV и создания сильного противовирусного иммунитета представляет собой интересный подход к разработке терапевтической вакцины. Вирусные векторы, используемые для этой цели, включают аденовирусные векторы (в основном нечеловеческие аденовирусные векторы, например, от шимпанзе), векторы вируса желтой лихорадки и векторы на основе модифицированного вируса осповакцины Анкара (MVA) [89,91,92].
Комбинация прайм-белка с последующей стимуляцией MVA, известная как TherVacB, оказалась очень успешной в различных доклинических моделях персистирующей инфекции HBV [59,91,93], что делает ее отличным кандидатом для стратегии терапевтической вакцинации для лечения HBV. . Ключевым преимуществом гетерологичной первичной бустерной вакцинации является индукция как CD8, так и CD4 Т-клеточного ответа. Поскольку Т-клетки CD4 играют важную роль в преодолении экспериментальной хронической инфекции и связаны с излечением хронического гепатита В у пациентов [18, 94], сопутствующая индукция противовирусного иммунитета против CD8 и CD4 Т-клеток может иметь решающее значение для эффективности вакцины. Различные комбинации первичных и бустерных вакцин в настоящее время проходят клинические испытания на эффективность в преодолении специфической иммунной толерантности к ВГВ и контроле над хроническим гепатитом В (таблица 1).

Необходимость индукции мощного HBV-специфического иммунитета для преодоления HBV-специфической толерантности в условиях хронического гепатита B [2,95] может быть лучше всего решена стратегиями гетерологичной вакцинации. Такие стратегии гетерологичной первичной бустерной вакцинации оказались полезными для повышения иммунитета при других вирусных инфекциях, таких как SARS-CoV-2 [96,97]. Текущие клинические испытания предоставят нам важную информацию о эффективности гетерологичной первичной терапевтической вакцинации у пациентов с хроническим гепатитом В.
5. Местная поддержка Т-клеточного иммунитета в печени для повышения эффективности терапевтической вакцинации
Печень обладает уникальными функциями как толерогенный орган [2, 29, 71, 98] и может ограничивать эффекторную функцию Т-клеток, генерируемых терапевтической вакцинацией, как только они распознают свой антиген в печени. Такую угрозу снижения эффективности терапевтической вакцинации невозможно устранить путем повышения иммуногенности терапевтической вакцинации, но могут потребоваться дополнительные меры, позволяющие эффекторным Т-клеткам локально в печени контролировать репликацию вируса и уничтожать инфицированные вирусом клетки. За последние несколько лет появились три разных подхода, которые потенциально могут повысить эффективность терапевтической вакцинации.
Комбинация терапевтической вакцинации с ингибированием передачи сигналов ко-ингибирующих рецепторов в Т-клетках может быть вариантом повышения эффективности вакцинации. Было показано, что экспрессия PD1 увеличивается в вирусспецифических Т-клетках при персистирующей инфекции различными вирусами, а блокада PD-1 повышает эффекторную функцию HBV-специфических Т-клеток у пациентов с хроническим гепатитом В или у доклинические модели [99–103]. Однако анти-PD-1 лечение пациентов с хроническим гепатитом В и гепатоцеллюлярной карциномой не выявило влияния ингибирования контрольных точек на восстановление HBV-специфического иммунитета и последующее снижение репликации вируса [104]. Несмотря на отсутствие восстанавливающего иммунитет эффекта анти-PD-1 терапии, комбинация терапевтической вакцинации с ингибированием контрольных точек может быть полезной для преодоления локального толерогенного микроокружения печени, где высок уровень экспрессии PD-L1. наблюдается [33,105]. В настоящее время в одном клиническом испытании изучается потенциал антитела против PD-1 в контексте терапевтической вакцинации у пациентов с хроническим гепатитом В (таблица 1).
Экспрессия антигена на высоком уровне была идентифицирована как ключевой фактор снижения эффективности ответа эффекторных Т-клеток [88, 106] и, как предполагается, играет роль в ослаблении HBV-специфического иммунитета при хронической инфекции [95, 106, 107]. Недавно мы продемонстрировали, что снижение репликации HBV и экспрессии генов с помощью подхода siRNA или shRNA перед терапевтической вакцинацией на двух разных моделях персистирующей HBV-инфекции у мышей повышает эффективность терапевтической вакцинации для элиминации HBV-экспрессирующих гепатоцитов и достижения контроля персистирующая инфекция [59]. Следует отметить, что ни индукция нейтрализующих антител, снижающих уровень циркулирующего HBsAg, ни опосредованный siRNA/shRNA нокдаун экспрессии гена HBV сами по себе не были способны восстановить HBV-специфический иммунитет [59]. Это подтверждает представление о том, что локальное ингибирование эффекторной функции Т-клеток в печени создает отдельное препятствие для Т-клеток, генерируемых терапевтической вакцинацией, для достижения контроля над персистирующей инфекцией.
Хотя печень известна своей толерогенной функцией и может ограничивать эффекторные функции Т-клеток, в печени может быть построен сильный иммунитет против патогенов, что, по-видимому, тесно связано с составом миелоидных клеток в печени [108]. В частности, замена толерогенных макрофагов печени (клеток Купфера) провоспалительными моноцитами коррелирует с индукцией иммунитета в печени [109]. Недавно была идентифицирована отдельная популяция клеток Купфера, которая способна перекрестно презентировать антигены, происходящие из гепатоцитов, Т-лимфоцитам CD8 при стимуляции IL -2 и, таким образом, повышать специфический к HBV иммунитет против инфицированных гепатоцитов [110].
Важно отметить, что накопление воспалительных моноцитов в печени в результате воспаления, вызванного TLR, приводит к массивной экспансии Т-клеток в печени в пределах выделенных анатомических ниш, называемых iMATE (агрегаты внутрипеченочных миелоидных клеток, связанные с экспансией Т-клеток) [111]. Т-клетки, размножающиеся внутри iMATE, обладают мощным эффекторным потенциалом и способны быстро уничтожать инфицированные вирусом гепатоциты [111]. Такое TLR-индуцированное и опосредованное миелоидными клетками увеличение количества эффекторных Т-клеток в печени также запускает элиминацию гепатоцитов, экспрессирующих трансгены, и устанавливает ответы памяти [112]. Недавно мы объединили терапевтическую вакцинацию и индукцию iMATE на модели персистирующей инфекции HBV у мышей.
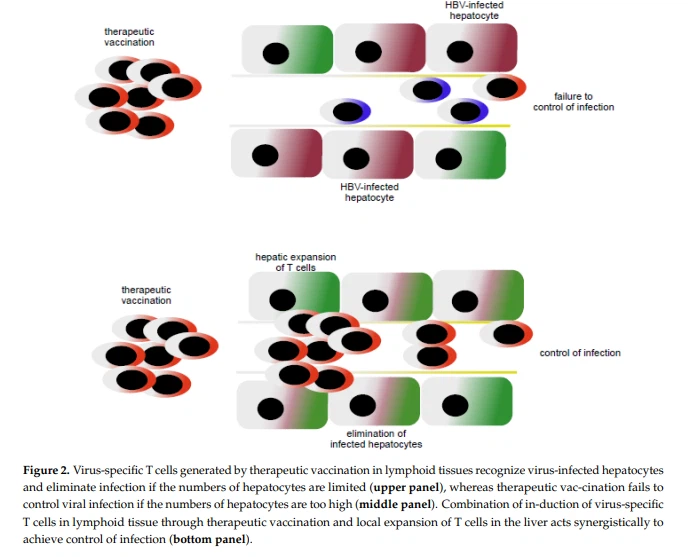
Комбинация гетерологичной прайм-буст-вакцинации (первичная вакцинация против антигена ВГВ с последующей бустерной вакцинацией MVA-ВГВ) с индукцией iMATE приводит к увеличению количества HBV-специфических эффекторных Т-клеток в печени [113]. Кроме того, он также повышает эффективность терапевтической вакцинации для элиминации HBV-экспрессирующих гепатоцитов из печени и устранения персистирующей инфекции [113]. Это демонстрирует синергическую активность терапевтической вакцинации с последующим локальным усилением Т-клеточного иммунитета в печени (см. Рисунок 2).

Высокое количество HBV-экспрессирующих гепатоцитов ограничивает эффективность гетерологичной первичной терапевтической вакцинации [91]. Способность комбинации терапевтической вакцинации с iMATE-индуцированной экспансией Т-клеток в печени контролировать инфекцию, более высокие уровни инфекции ВГВ, чем при контроле только терапевтической вакцинацией, еще больше укрепляет представление о том, что терапевтическая вакцинация продуцирует большое количество вирус-специфических эффекторных Т-лимфоцитов. клетки, предположительно во вторичных лимфоидных тканях, и локальная экспансия Т-клеток в печени представляют собой два отдельных механизма, которые синергически повышают эффективность терапевтической вакцинации против инфицированных вирусом гепатоцитов в печени.
Таким образом, стратегии гетерологичной первичной бустерной вакцинации используют синергетические принципы для повышения эффективности вакцинации против хронических вирусных инфекций. Возможности для дальнейшего повышения эффективности вакцины могут заключаться в сочетании локального усиления индуцированных вакциной иммунных ответов, таких как упомянутое выше усиление индуцированного вакциной Т-клеточного иммунитета за счет увеличения силы Т-клеточного иммунитета локально в печени. Кроме того, улучшение стратегий нацеливания и доставки в печень молекул, повышающих Т-клеточный иммунитет в печени, может обеспечить дополнительные преимущества для преодоления иммунной толерантности при хроническом воспалении.

Вклад автора:
Концептуализация, ПАК и УП; написание – черновая подготовка, ПАК; написание — рецензирование и редактирование, L.-RH, AK, DW и UP Все авторы прочитали и согласились с опубликованной версией рукописи.
Финансирование:
Это исследование финансировалось Немецким исследовательским фондом (DFG), номер гранта 272983813-TRR179.
Заявление Институционального контрольного совета:
Непригодный.
Заявление об информированном согласии:
Непригодный.
Заявление о доступности данных:
Непригодный.

Конфликт интересов:
Авторы объявили, что нет никаких конфликтов интересов.
Рекомендации
1. Маклахлан, Дж. Х.; Коуи, BC Эпидемиология вируса гепатита В. Харб Колд Спринг. Перспектива. Мед. 2015, 5, а021410. [Перекрестная ссылка] [PubMed]
2. Процер, У.; Майни, МК; Knolle, PA Жизнь в печени: печеночные инфекции. Нац. Преподобный Иммунол. 2012, 12, 201–213. [Перекрестная ссылка]
3. Нолл, Пенсильвания; Тимме, Р. Иммунная регуляция печени и ее участие в инфекции вирусным гепатитом. Гастроэнтерология 2014, 146, 1193–1207. [Перекрестная ссылка]
4. Тимме Р.; Виланд, С.; Стайгер, К.; Грейеб, Дж.; Рейманн, К.А.; Перселл, Р. Х.; Chisari, FV CD8(plus) Т-клетки опосредуют клиренс вируса и патогенез заболевания во время острой вирусной инфекции гепатита В. Дж. Вирол. 2003, 77, 68–76. [Перекрестная ссылка]
5. Лю, Дж.; Ян, привет; Ли, Массачусетс; Лу, С.Н.; Джен, CL; Ван, LY; Вы, С.Л.; Илоехе, штат Массачусетс; Чен, СиДжей; Группа, R.-HS Заболеваемость и детерминанты спонтанного сероклиренса поверхностного антигена гепатита В: последующее исследование на уровне сообщества. Гастроэнтерология 2010, 139, 474–482. [Перекрестная ссылка]
6. Нассал, М. кзкДНК вируса гепатита В: резервуар персистенции вируса и основное препятствие для лечения хронического гепатита В. Gut 2015, 64, 1972–1984. [Перекрестная ссылка]
7. Вэй, Л.; Плосс, А. Механизм образования кзкДНК вируса гепатита В. Вирусы 2021, 13, 1463. [CrossRef] [PubMed]
8. Павлоцкий, Дж.; Негро, Ф.; Агемо, А .; Беренгер, М .; Далгард, О .; Душейко Г.; Марра, Ф.; Пуоти, М.; Wedemeyer, H. Рекомендации EASL по лечению гепатита C: Окончательное обновление серии. Дж. Гепатол. 2020, 73, 1170–1218. [Перекрестная ссылка] [PubMed]
9. Линденбах, Б.Д.; Райс, К.М. Преодоление репликации вируса гепатита С от генома до функции. Природа 2005, 436, 933–938. [Перекрестная ссылка] [PubMed]
10. Люцифора, Дж.; Ся, Ю .; Райзингер, Ф .; Чжан, К .; Стадлер, Д.; Ченг, X .; Спринцл, М.Ф.; Коппенштайнер, Х .; Маковска, З.; Волц, Т .; и другие. Специфическая и негепатотоксическая деградация кзкДНК ядерного вируса гепатита В. Наука 2014, 343, 1221–1228. [Перекрестная ссылка] [PubMed]
11. Олвейс, Л.; Дандри, М. Роль кзкДНК в поддержании HBV. Вирусы 2017, 9, 156. [CrossRef]
12. Люцифора, Дж.; Protzer, U. Атака кзкДНК вируса гепатита B – Святой Грааль для лечения гепатита B. Дж. Гепатол. 2016, 64, С41–С48. [Перекрестная ссылка]
13. Цунис, Е.П.; Туркохристу, Э.; Музаки, А .; Триантос, К. На пути к новой эре терапии вируса гепатита В: стремление к функциональному излечению. Мировой Ж. Гастроэнтерол. 2021, 27, 2727–2757. [Перекрестная ссылка]
14. Мартинес, М.Г.; Виллере, Ф.; Тестони, Б.; Зоулим, Ф. Можем ли мы вылечить вирус гепатита В с помощью новых противовирусных препаратов прямого действия? Печень инт. 2020, 40 (Прил. 1), 27–34. [Перекрестная ссылка]
15. Нагги, С.; Лок, А.С. Новые методы лечения гепатита В: путь к излечению. Анну. преподобный мед. 2021, 72, 93–105. [Перекрестная ссылка] [PubMed]
16. Урбан, С.; Нейманн-Хефелин, К.; Лампертико, П. Вирус гепатита D в 2021 г.: вирусология, иммунология и новые подходы к лечению трудноизлечимого заболевания. Гут 2021, 70, 1782–1794. [Перекрестная ссылка]
17. Рехерманн, Б.; Nascimbeni, M. Иммунология вируса гепатита B и инфекции вируса гепатита C. Нац. Преподобный Иммунол. 2005, 5, 215–229. [Перекрестная ссылка] [PubMed]
18. Ван, Х.; Луо, Х .; Ван, X .; Фу, Х .; Мао, Q .; Сян, X .; Чжоу, Ю .; Он, В .; Чжан, Дж.; Го, Ю .; и другие. Профиль ФНО-альфа/ИФН-гамма HBV-специфических CD4 T-клеток связан с повреждением печени и элиминацией вируса при хронической инфекции HBV. Дж. Гепатол. 2020, 72, 45–56. [Перекрестная ссылка] [PubMed]
19. Гилл, США; Маккарти, NE CD4 Т-клетки в вирусе гепатита В: «Вам не обязательно быть цитотоксичными, чтобы работать здесь и помогать». Дж. Гепатол. 2020, 72, 9–11. [Перекрестная ссылка]
20. Rehermann, B. Патогенез хронического вирусного гепатита: дифференциальная роль Т-клеток и NK-клеток. Нац. Мед. 2013, 19, 859–868. [Перекрестная ссылка]
For more information:1950477648nn@gmail.com
