KidneyNetwork: использование данных экспрессии генов, полученных из почек, для прогнозирования и определения приоритетов новых генов, участвующих в заболевании почек Ⅰ
Aug 07, 2023
Генетическое тестирование у пациентов с подозрением на наследственнуюболезнь почекможет не выявить генетическую причину расстройства, поскольку потенциально патогенные варианты могут находиться в генах, участие которых еще не известно.болезнь почек. Мы разработали Kidney Network, в которой используется тканеспецифическая экспрессия для информирования о приоритетах генов-кандидатов специально для заболеваний почек. KidneyNetwork — это новый метод, созданный путем интеграции сети совместной экспрессии почечной РНК из 878 образцов с мультитканевой сетью из 31 499 образцов. Он использует паттерны экспрессии и установленные ассоциации ген-фенотип, чтобы предсказать, какие гены могут быть связаны с какими фенотипами (заболеванием) беспристрастным образом. Мы применили KidneyNetwork к редким вариантам данных секвенирования экзома у 13 пациентов с заболеванием почек без генетического диагноза, чтобы определить приоритет генов-кандидатов. KidneyNetwork может точно прогнозировать функции генов, специфичных для почек, и фенотипы (заболевания почек) для генов, связанных с заболеванием. Пересечение приоритетных генов с генами, несущими редкие варианты у пациента с кистами почек и печени, определило ALG6 как вероятный ген-кандидат. Мы усиливаем эту правдоподобность, идентифицируя варианты ALG6 в нескольких случаях кистозных заболеваний почек и печени без альтернативных генетических объяснений. Мы представляем KidneyNetwork, общедоступную сеть коэкспрессии, специфичную для почек, с оптимизированными предсказаниями фенотипов генов для фенотипов заболеваний почек.

Мы разработали простой в использовании онлайн-интерфейс, который позволяет клиницистам и исследователям использовать данные об экспрессии генов и совместной регуляции, а такжесвязи генов и фенотипов для ускорения прогресса в диагностике и исследованиях наследственных заболеваний почек.
ЗАЯВЛЕНИЕ О ПЕРЕВОДЕ:Генетическое тестирование у пациентов с подозрением на наследственнуюболезнь почекможет не выявить генетическую причину расстройства пациента. Потенциально патогенные варианты могут находиться в генах, о которых еще не известно, что они связаны с заболеванием почек, что затрудняет интерпретацию значимости этих вариантов. Это показывает явную потребность в методах для беспристрастного прогнозирования фенотипических последствий генетической изменчивости. Здесь мы описываем KidneyNetwork, инструмент, который использует тканеспецифическую экспрессию для прогнозирования функций генов, специфичных для почек. Применение KidneyNetwork к группе невыявленных случаев определило ALG6 как ген-кандидат в кистозной почке иболезнь печени. Таким образом, KidneyNetwork может помочь в интерпретации генетических вариантов и, следовательно, может быть ценным в трансляционном нефрогенезе и помочь улучшить диагностический результат у пациентов с заболеваниями почек.

НАЖМИТЕ ЗДЕСЬ, ЧТОБЫ ПОЛУЧИТЬ CISTANCHE ДЛЯ ПОЧКИБОЛЕЗНЬ
ВВЕДЕНИЕ
Генетическое тестирование у пациентов с подозрением на наследственную болезнь почек может выявить этиопатогенные варианты вгены, связанные с почками. Однако во многих случаях генетическая причина еще не может быть обнаружена. Патогенные варианты в известных почечных генах обнаруживаются примерно у 10–30% генетически протестированных пациентов с хроническим заболеванием почек любой этиологии [1–3]. Однако эти проценты, вероятно, являются недооценкой числа пациентов с моногенной причиной, поскольку варианты в генах, еще не вовлеченные в заболевание почек, останутся незамеченными. В этих генах могут находиться потенциально опасные варианты, что затрудняет определение приоритетов и интерпретацию релевантности этих вариантов. Поэтому в нынешнюю эпоху геномной медицины одной из основных задач после отрицательного результата диагностики в известных генах является обнаружение и приоритизация новых генов-кандидатов с потенциально патогенными вариантами, которые могут объяснить заболевание пациента [4].
Данные секвенирования РНК можно использовать для прогнозирования кандидатагены болезни[5]. Недавно мы разработали GeneNetwork и метод GeneNetwork-Assisted Diagnostic Optimization (GADO) для определения приоритетов новых генов-кандидатов болезней на основе данных секвенирования РНК [6]. Идея этого метода заключается в том, что некоторые редкие заболевания могут быть вызваны вариантами в нескольких генах. Хотя эти гены различны, они обычно имеют схожие биологические функции. При изучении данных экспрессии генов из большого количества образцов эти гены заболеваний обычно демонстрируют сильную коэкспрессию [6]. Таким образом, если есть другие гены, которые сильно коэкспрессируются с известными генами редких заболеваний, возможно, что варианты в этих других генах также могут вызывать то же заболевание.
Для оптимальной работы такого инструмента информация о совместном выражении должна быть максимально точной. Для GADO мы построили сеть коэкспрессии генов на основе общедоступных наборов данных секвенирования РНК из разных тканей и использовали эту сеть, чтобы предсказать, какие гены могут вызывать редкие заболевания. Эти прогнозы были обучены с использованием базы данных онтологии фенотипов человека (HPO) [7]. В базе данных HPO гены отнесены к фенотипам, называемым терминами HPO, которые основаны на аннотациях генов и симптомов заболевания, представленных в базах данных OMIM [8] и Orphanet [9]. Интегрируя информацию из базы данных HPO с сетью совместной экспрессии генов, мы могли рассчитать прогнозные баллы для каждого гена на термин HPO. Вместе эти оценки составляют GeneNetwork. Затем GADO определяет приоритеты генов, комбинируя входной список терминов HPO, описывающих фенотип пациента, со списком генов с возможными вредными вариантами этого пациента. Приоритизация списка генов основана на комбинированных оценках предсказания генов для входных терминов HPO [6].
Поскольку мы заметили, что эффективность предсказания GeneNetwork для фенотипов HPO, связанных с почками, была ограниченной, мы стремились улучшить предсказание, разработав сеть, специфичную для почек. Мы сделали это, используя 878 образцов секвенирования почечной РНК, которые мы обогатили существующим набором данных из 31 499 образцов из других тканей [6]. Разработав новый алгоритм прогнозирования, который может взвешивать информацию, присутствующую в обоих наборах данных, мы улучшили производительность путей, связанных с почками. В этой статье мы представляем полученную KidneyNetwork, коэкспрессионную сеть, которую можно использовать для точного предсказания фенотипических ассоциаций генов, неизвестных для связанных с почками терминов HPO. В качестве доказательства принципа мы применили KidneyNetwork к данным секвенирования экзома у группы пациентов с ранее нерешенными заболеваниями почек.
МЕТОДЫ
Чтобы улучшить прогнозирование фенотипов, связанных с почками, мы собрали данные секвенирования РНК, полученные из почек, обновили GeneNetwork с помощью более свежих справочных баз данных и улучшили статистический анализ с последующей интеграцией тканеспецифической информации.
Наборы данных в KidneyNetwork
Данные секвенирования РНК из выбранных образцов почек различного происхождения, включая первичную, опухолевую и эмбриональную ткань, были объединены с существующим набором данных секвенирования РНК из нескольких тканей, использованным в качестве основы для нашей ранее описанной GeneNetwork [6] (таблица S1, S2). . Мы решили включить набор данных с несколькими тканями по двум причинам. Во-первых, нам нужно было достаточное количество образцов для построения базовой сети. Во-вторых, мы хотели сохранить экспрессию, специфичную для нескольких или всех типов клеток почек, но не для других тканей. Мы сделали это, потому что оценки гена-фенотипа основаны на различиях в экспрессии между образцами; если все гены имеют высокую (или низкую) экспрессию во всех образцах, включенных в анализ, они не добавят достаточной информации в алгоритм предсказания. Набор данных о нескольких тканях образцов секвенирования РНК человека, использованный для разработки GeneNetwork, был повторно использован и обработан, как описано ранее [6]. После предварительной обработки этот набор данных содержал 31 499 образцов и 56 435 генов.
3194 образца секвенированной РНК, полученной из почек, были загружены из Европейского архива нуклеотидов (ENA) и проекта экспрессии генотипа-ткани (GTEx) (примечание S1). Предварительная обработка набора данных о почках проводилась аналогично набору данных о нескольких тканях [6] (примечание S2, примечание S3). После отбора образцов и генов осталось 58 283 гена и 878 образцов почек. Мы исследовали оставшиеся 878 образцов секвенирования РНК, используя алгоритм кластеризации UMAP (примечание S4).
Фильтрация ГПО. Для построения KidneyNetwork мы использовали ассоциации ген-фенотип из базы данных HPO [7], версия 1268. В базе данных HPO аннотации генов к фенотипам, определяемым HPO, основаны на аннотациях генов-заболеваний в OMIM [8] morbid. карта (загружена 26 марта 2018 г.) и файл Orphanet [9] "en_product6.xml" версии 1.3.1. Аннотации ген-заболевание в этих базах данных могут быть основаны на нескольких факторах, включая статистические ассоциации и крупномасштабные вариации числа копий. Мы хотели обучить KidneyNetwork, используя только те гены, для которых хорошо установлена связь между геном и редким заболеванием. Поэтому мы исключили мультигенные синдромы, так как часто неясно, какие гены в вариантах числа копий вносят вклад в какие фенотипы. Мы также исключили простые гены восприимчивости (Примечание S5).
Нормализация выражения. После контроля качества образцов и генов (QC) матрица экспрессии оставшихся образцов и генов была преобразована в log2-, а количество генов было нормализовано с использованием DESeq в соответствии с методом медианы отношений. Затем мы скорректировали данные экспрессии генов для ковариатов (Примечание S6).

Разложение
После фильтрации и контроля качества всего набора данных следующим шагом было выполнение декомпозиции для вычисления собственных векторов набора данных (Примечание S7). Как для GeneNetwork, так и для регуляторной сети генов на основе данных, полученных из почек, мы определили оптимальное количество компонентов (Примечание S8). Первые 165 собственных векторов для GeneNetwork и первые 170 собственных векторов для данных, полученных из почек, были идентифицированы и объединены в большую матрицу, содержащую все 335 собственных векторов.
Расчет оценки ген-HPO-term Расчет оценки ген-фенотип выполнялся в несколько этапов (рис. S5). Во-первых, мы выполнили логистическую регрессию, используя объединенные собственные векторы и файл аннотаций ген-фенотип в качестве входных данных. Мы использовали полученные значения и оценки собственных векторов для расчета оценки логарифмических шансов генов для каждого гена в каждом собственном векторе (Примечание S9).

Чтобы избежать переобучения логарифмических шансов уже аннотированных генов, мы применили подход перекрестной проверки с исключением одного (Примечание S10). Затем логарифмические шансы были переведены в z-значения генов с использованием пермутированного нулевого распределения для каждого фенотипа (примечание S11).
Чтобы определить точность прогноза, мы рассчитали площадь под ROC-кривой (AUC). AUC рассчитывали на термин HPO с использованием предсказанных z-показателей гена и известных аннотаций. Значимость прогнозов рассчитывали с использованием двустороннего рангового теста Манна-Уитни. После поправки Бонферрони прогноз считался значимым при p < 0,05.
Сравнение эффективности прогнозирования
Мы сравнили эффективность прогнозирования четырех различных сетей: (1) исходной GeneNetwork, (2) обновленной GeneNetwork, (3) сети регуляции специфичных для почек генов, основанной исключительно на образцах, полученных из почек, и, наконец, (4) KidneyNetwork, которая объединяет последние два. Качество прогнозов HPO, сделанных этими сетями, оценивалось на основе AUC для каждого фенотипа, связанного с почками (таблица S3). Улучшенное качество сети определялось как повышенная точность предсказания для терминов, связанных с почками, которые были достоверно предсказаны при каждом сравнении двух сетей, а также за счет увеличения числа значимо предсказанных терминов, связанных с почками. Значимость улучшения точности предсказания одной сети по сравнению с другой оценивалась с помощью теста Делонга [10], интегрированного в пакет pROC R [11].
Применение KidneyNetwork у 13 пациентов с подозрением на наследственное заболевание почек Одним из применений KidneyNetwork является определение приоритетности генов-кандидатов у пациентов с нерешенным заболеванием почек. Чтобы оценить это клиническое применение, мы использовали KidneyNetwork для определения приоритетов генов-кандидатов для пациентов с различными заболеваниями почек с использованием метода GADO [6]. GADO объединяет z-показатели предсказания генов, полученные через KidneyNetwork для заданного набора терминов HPO. Гены с комбинированным z-показателем больше или равным 5 для уникального набора терминов HPO, связанных с каждым пациентом, считались потенциальными генами-кандидатами для этого пациента.

Рис. 1 UMAP-визуализация данных экспрессии, полученных из почек. 878 образцов были сгруппированы в три основных кластера: здоровая первичная ткань (средний и нижний), образцы развития (слева) и образцы почечно-клеточного рака (ПКР) (справа). В левой части рисунка можно увидеть скопление подоцитов, полученных из плюрипотентных стволовых клеток (PSC), и органоидов, полученных из PSC, с первичными фетальными образцами и клетками-предшественниками нефрона. С правой стороны образцы ПКР сгруппированы рядом с образцами проксимальных канальцев, а кластер ПКР, ближайший к образцам здоровой первичной ткани, состоит из образцов ПКР с несветлыми клетками (нзПКР). В середине и внизу образцы здоровых первичных почек сгруппированы в зависимости от ткани их происхождения.
У всех 13 пациентов, включенных в исследование, было подозрение на моногенное заболевание почек, но у них не было генетического диагноза (примечание S12). Термины HPO были присвоены этим случаям на основе их фенотипа. Для каждого пациента полные данные секвенирования экзома были проанализированы с помощью CAPICE [12] для выявления потенциально патогенных вариантов. Гены, содержащие варианты с АФ фильтрации gnomAD Popmax [13]<0.005 and a recall ≥99%, corresponding with a mild CAPICE cut-off of ≥0.0027, were considered interesting candidates.
Перекрытие генов, идентифицированных интеграцией KidneyNetwork в GADO, с генами, идентифицированными CAPICE, привело к созданию списка генов для каждого пациента. Эти гены и варианты в этих генах были вручную рассмотрены группой экспертов по нефрогенезу (AMvE, LRC, NVAMK) на предмет их патогенетического потенциала на основе показателей популяции, инструментов прогнозирования, доступной литературы и сегрегации (Примечание S13). Для полученного гена-кандидата дополнительные пациенты, несущие варианты в том же гене, были идентифицированы с помощью сотрудников и проекта 100, 000 Genomes [14]. Кроме того, использовался инструмент GeneMatcher [15], который не дал дополнительных пациентов до 15 февраля 2023 года.
Идентификация дополнительных пациентов Ранее описанная когорта с нерешенным поликистозом почек и печени [16] использовалась для оценки редких вариантов (Примечание S14). Мы использовали точный критерий Фишера для сравнения частоты идентифицированных вариантов с европейской подгруппой нефинских европейцев в базе данных gnomAD [17]. Кроме того, мы использовали проект 100,000 Genomes [14] для идентификации дополнительных пациентов на основе идентифицированных вариантов (вариантов) (примечание S15).

ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ
Поиск данных и кластеризация образцов Мы отобрали 878 образцов почек (рис. S2), которые мы кластеризовали и нанесли на график с использованием алгоритма UMAP (рис. 1). Как правило, данные объединяются в три основных группы: первичные неопухолевые данные о почках, образцы развития почек и образцы проксимальных канальцев, клубочков и почечно-клеточной карциномы (ПКР).
KidneyNetwork улучшает предсказания гено-фенотипа Во-первых, мы обновили GeneNetwork обновленной базой данных HPO (рис. S6) и оптимизировали конвейер построения генной сети (рис. S7). Эти изменения привели к улучшению общей GeneNetwork по сравнению с предыдущей версией (рис. S8). Затем мы использовали улучшенный конвейер для создания регуляторной сети генов, специфичных для почек. Как и ожидалось, учитывая небольшой размер выборки, эта версия почечной сети работала хуже, чем GeneNetwork (рис. S9). Впоследствии объединение GeneNetwork и сети коэкспрессии генов, специфичных для почек, в KidneyNetwork дало наши наилучшие результаты для терминов HPO, связанных с почками (рис. 2A; таблица S5). Предусмотрены прогнозируемая AUC, точность, чувствительность и f1-показатели для каждого прогнозируемого пути (таблица S6).
Двумя примерами улучшенных терминов HPO, связанных с почками, являются гипомагниемия и тубулоинтерстициальная аномалия (рис. 2B). Визуализация этих фенотипов на графиках плотности показывает более высокие z-показатели приоритета для известных генов, связанных с заболеванием, по сравнению с неаннотированными генами. Для неизвестных генов, чем выше прогнозируемый z-показатель, тем больше вероятность того, что они являются геном-кандидатом болезни. Визуализация сетей взаимодействия генов известных генов болезней на основе оценок прогнозирования снова показывает увеличение количества и силы взаимодействий, полученных с использованием KidneyNetwork, по сравнению с GeneNetwork.
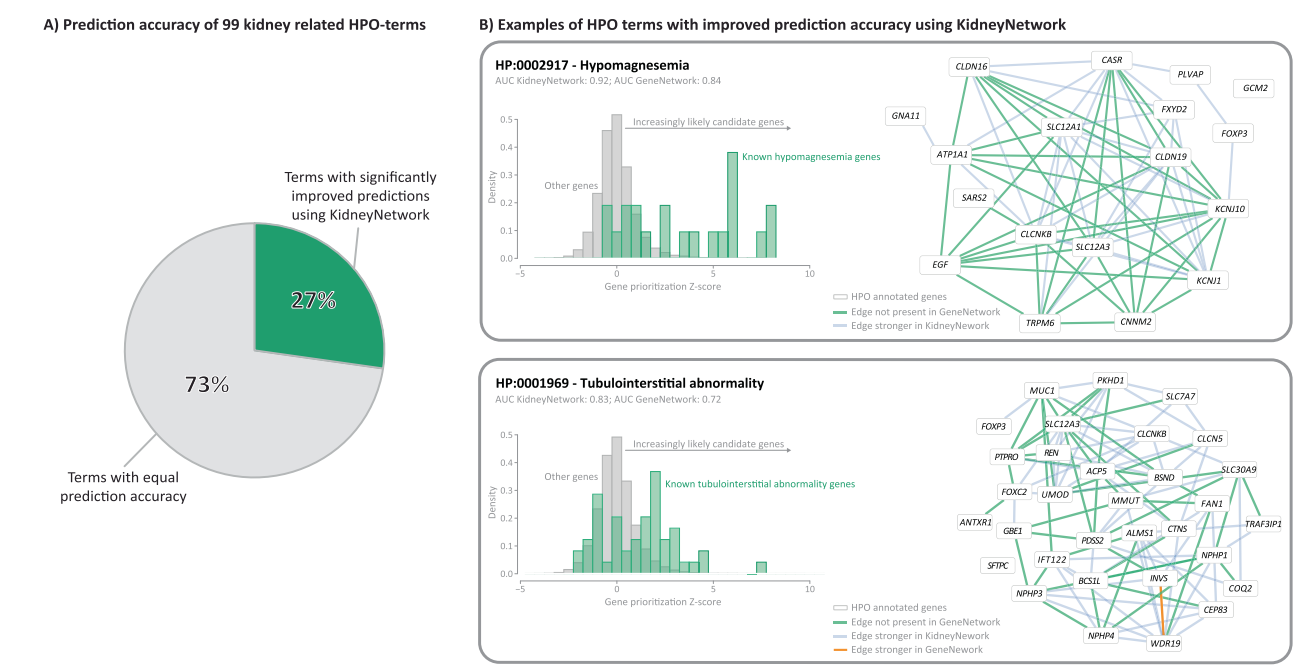
Рис. 2. KidneyNetwork работает лучше для терминов HPO, связанных с почками, чем обновленная GeneNetwork. 27 процентов фенотипов, связанных с почками, прогнозируются значительно лучше с использованием KidneyNetwork по сравнению с GeneNetwork. B Графики плотности оценок предсказания генов в пределах двух из наиболее улучшенных фенотипов, гипомагниемии и тубулоинтерстициальной аномалии, показывают более высокие значения предсказания для генов, аннотированных для фенотипа, а также предсказывают потенциальные неизвестные гены-кандидаты. Сети, предсказанные с помощью KidneyNetwork, показывают более сильные корреляции между аннотированными генами, чем сети, предсказанные с помощью GeneNetwork.
Мы также увидели увеличение количества значимых предсказанных терминов HPO, связанных с почками, для KidneyNetwork (n=71) по сравнению с GeneNetwork (n=63). Это привело нас к гипотезе о том, что KidneyNetwork предсказывает термины, связанные с почками, с более высокой точностью в целом и, следовательно, способен предсказывать больше фенотипов, связанных с почками, с более высокой значимостью. Парный t-критерий показывает, что в целом оценка AUC HPO была значительно лучше для KidneyNetwork по сравнению с GeneNetwork (средняя AUC: 0,76 по сравнению с 0,74; p-значение t-критерия: 4,5 × 10 −8 ). Этот результат предполагает, что KidneyNetwork предсказывает больше специфичных для почек терминов HPO с более высокой точностью предсказания, чем GeneNetwork.
KidneyNetwork отдает приоритет ALG6 в качестве гена-кандидата заболевания у пациентов с кистами почек и кистами печени. Чтобы изучить клиническую полезность KidneyNetwork, мы определили приоритеты генов для 13 пациентов с подозрением на наследственное заболевание почек, но без генетического диагноза, и пересекли их с генами, содержащими потенциально патогенные варианты. Полученные списки генов содержали от 1 до 4 генов-кандидатов для 9 из 13 пациентов (таблица S7). У одного пациента (SAMPLE6) ручное курирование этого списка определило ALG6 (ALG6 альфа-1,3-глюкозилтрансфераза) в качестве потенциального гена-кандидата для объяснения кист почек и печени пациента (рис. 3). Комбинированный z-показатель для ALG6 для вмененных терминов HPO был значительным в KidneyNetwork после множественной коррекции тестирования (z=5,43). Этот ген был бы упущен, если бы мы использовали GeneNetwork: там ALG6 не достиг порога значимости z-показателя больше или равного 5.

ALG6 как ген-кандидат для пациентов с кистами почек и печени Вариант ALG6 c.680 плюс 2 T > G, переносимый SAMPLE6, является гетерозиготным. Это известный патогенный вариант сайта сплайсинга, который приводит к врожденному нарушению гликозилирования (CDG) типа Ic, когда патогенные варианты присутствуют на обоих аллелях [18, 19]. ALG6 сильно напоминает ALG8, который участвует в фенотипах кист почек и печени [20], и, согласно KidneyNetwork, ALG6 и ALG8 сильно корегулируются (z-показатель=8,59).
Учитывая эту биологическую достоверность, мы опросили когорту из 12 0 неродственных случаев поликистоза почек и печени на наличие редких вариантов, MAF < 0.001, в ALG6. Эта когорта незначительно обновлена, так как она была описана ранее, и была исключена с помощью анализа секвенирования экзома на предмет мутаций с потерей функции или сообщений о патогенных неусеченных вариантах в PKD1, PKD2, PRKCSH, SEC63, GANAB, ALG8, ALG9, SEC61B, PKHD1 или ДНКJB11 [16]. Три несвязанных случая (YU372, YU378, YU481) несли редкие варианты ALG6; каждый из них имел один и тот же ALG6 c.257 плюс 5G > неканонический вариант сплайсинга, который, как известно, является патогенным для ALG6-CDG и изменяет сплайсинг in vitro [19, 21]. Несмотря на общую мутацию, в каждом из этих трех случаев сообщается об отсутствии известных пораженных членов семьи, зарегистрированных в разных штатах США, и они не связаны с наилучшим пределом обнаружения с использованием алгоритма связанности2 VCFtools с родственностью _PHI < 0,005.
Учитывая представленность этого варианта в трех случаях европейского происхождения в этой фенотипически определенной когорте, мы сравнили его частоту в европейском подмножестве случаев (n=105) с нефинскими европейцами в gnomAD [17] с охватом в эта позиция (n=64, 466) [17]. В когорте пациентов 3 из 210 аллелей содержали этот вариант, в то время как в gnomAD, когорте, не отобранной в отношении кисты почек или печени, он был обнаружен в 121 из 128 932 аллелей. Это приблизительно 10-кратное обогащение является статистически значимым по точному критерию Фишера, p=0,0011. Эта мутация также повторялась в случаях ALG6-CDG [19].
Мы также исследовали набор данных 100,000 Genomes Project [14] и связались с сотрудниками, которые определили три дополнительных данных для применения к заболеваниям почек. Значительная часть пациентов с подозрением на генетическое заболевание почек остается без генетического диагноза, так как списки генов заболеваний для многих состояний неполные. Выявление того, какие гены вовлечены в заболевание почек, имеет важное значение для улучшения результатов диагностики у пациентов с заболеванием почек и для изучения патогенеза заболевания, чтобы приблизиться к методам лечения. Установление новых генов болезней требует тщательной биологической проверки. Вовлечение генов, достойных таких исследований, имеет решающее значение. Применение KidneyNetwork в сочетании с данными WES или GWAS нефрологами, клиническими генетиками или исследователями поможет каждой из этих групп участвовать в импликации генов. KidneyNetwork объединяет сеть совместной экспрессии, основанную на наборе данных образцов почек, с ранее опубликованным набором данных о нескольких тканях, который использовался для построения работы GeneNet. Объединение наборов данных в KidneyNetwork улучшило прогнозы фенотипов, связанных с заболеванием почек, по сравнению с сетями, основанными на двух наборах данных по отдельности. В качестве доказательства принципа мы показываем, что список генов-кандидатов для комбинированного фенотипа кист почек и печени, созданный KidneyNetwork, имеет приоритет над управляемым списком генов-кандидатов из длинного списка генов, содержащих редкие варианты у нашего пациента с этим фенотипом.
Мы также исследовали набор данных 100,000 Genomes Project [14] и связались с сотрудниками, которые выявили еще трех пациентов с кистами почек и/или печени, несущих гетерозиготный потенциально опасный вариант ALG6, без альтернативного генетического объяснения.

Рис. 3 KidneyNetwork, включенная в метод GADO в SAMPLE6, у пациента с почечными и печеночными кистами. KidneyNetwork приоритизировала 89 генов-кандидатов из всех генов с использованием GADO на основе терминов HPO «кисты почек» (HP: 0000107) и «кисты печени» (HP: 0001407). Метод интерпретации данных секвенирования экзома CAPICE выявил 322 гена, содержащих потенциально патогенные варианты, в данных секвенирования экзома пациента. При перекрытии этих списков генов были идентифицированы три гена, которые соответствовали критериям отбора, одним из которых был ALG6.
В общей сложности мы идентифицировали семь пациентов с известными вариантами сайта сплайсинга, которые, как сообщалось, вызывали заболевание у пациентов с тяжелым поражением CDG при гомозиготности или сложной гетерозиготности, и одного пациента с вероятным патогенным вариантом сайта сплайсинга (таблица 1). В отличие от тяжело пораженных пациентов с ALG6-CDG (с поражением нескольких органов, включая задержку развития и множественные неврологические симптомы), у наших пациентов был фенотип множественных кист почек и/или кист печени (рис. 4). . В то время как PCLD может быть обширным, почечный фенотип, по-видимому, является легким, без сообщений о снижении рСКФ, несмотря на пожилой возраст (например, одному пациенту за тридцать, другим от 45 до 80 лет). Кроме того, мы обнаружили, что вариант ALG6 сегрегировался у нескольких членов семьи, которые также были поражены (таблица 1; рис. 4).
Служба поддержки:
Электронная почта: wallence.suen@wecistanche.com
Whatsapp/тел.: плюс 86 15292862950
Магазин:
https://www.xjcistanche.com/cistanche-shop






