Часть Ⅱ Роль повреждения митохондриальной ДНК при заболеваниях почек: новый биомаркер
Jun 13, 2023
Распределение мтДНК при заболеваниях почек
Как правило, интактная мтДНК присутствует в митохондриальном матриксе, но не присутствует в клеточном матриксе, периферической крови или моче. Однако повреждение митохондрий способствует повреждению клеток при множественных заболеваниях и часто сопровождается утечкой мтДНК из митохондрий, когда утечка мтДНК недостаточна для очистки с помощью системы клеточного восстановления и фагоцитоза, они могут высвобождаться в периферический кровоток. мтДНК в периферическом кровотоке фильтруется через барьер клубочковой фильтрации и участвует в образовании мочи. Отслойка клеток в мочевыделительной системе, такой как мочевой пузырь и мочеточник, также может приводить к присутствию мтДНК в моче. Следовательно, мтДНК можно обнаружить как в периферической плазме, так и в моче. Уровни мтДНК в периферической крови и моче можно использовать для оценки функции митохондрий и состояния некоторых органов. Также растет число исследований корреляций между распределением мтДНК и функцией почек (рис. 3).
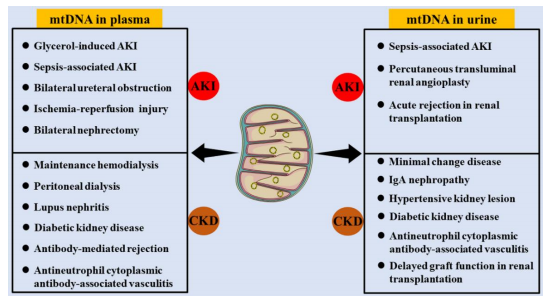
Рисунок 3. Распределение мтДНК при заболеваниях почек. мтДНК может быть обнаружена как в периферической плазме, так и в моче при множественных заболеваниях почек, включая ОПП и ХБП. (ОПП, острая почечная недостаточность; ХБП, хроническая болезнь почек; IgA, иммуноглобулин А).
1. мтДНК в периферической сыворотке
Уровни мтДНК в периферической сыворотке относительно низки при нормальных физиологических условиях, и ее концентрация увеличивается при повреждении нескольких органов или тканей, таких как почки, сердце, печень, мозг и мышцы [55–58]. Сообщалось о корреляции между мтДНК плазмы и заболеваниями почек, включая ОПП и ХБП. Кроме того, мтДНК плазмы считается индикатором для оценки повреждения почек.
Многочисленные факторы могут спровоцировать возникновение ОПП, в том числе двусторонняя обструкция мочеточников, сепсис-ассоциированный ОПП, индуцированный глицерином ОПП, ишемически-реперфузионное повреждение (ИРИ) и двусторонняя нефрэктомия [59]. Была принята во внимание прогностическая роль мтДНК плазмы при ОПП. Например, уровень мтДНК в плазме был повышен у больных ОПП с сепсисом [60]. У крыс с индуцированным глицерином ОПП концентрация мтДНК в плазме повышалась через 3 часа, что указывает на то, что мтДНК в плазме может быть ранним и чувствительным биомаркером ОПП [61].
В более позднем исследовании когорты с хронической почечной недостаточностью сообщалось, что более низкое число копий мтДНК коррелировало с более высоким риском прогрессирования ХБП, независимо от установленных факторов риска у пациентов с ХБП [62]. Высвобождение мтДНК в тромбоцитах, управляемое рецептором иммунного комплекса Fc RIIA, является ключевым источником митохондриальных антигенов при системной красной волчанке [7]. Накачивая избыток мтДНК в кровоток мышей, высокий уровень мтДНК в сыворотке может вызвать воспаление и вызвать повреждение почек [63]. Плазменная мтДНК является сильным предиктором сердечно-сосудистых событий, а также необходимости госпитализации у пациентов на перитонеальном диализе [64]. У пациентов, находящихся на поддерживающем гемодиализе (МГД), содержание циркулирующей мтДНК было значительно выше у пациентов с саркопенией вместе с более высокой экспрессией TLR9 и IL-6, что продемонстрировало, что мтДНК может быть вовлечена в патогенез саркопении, связанной с МГД [65]. . Как один из незаменимых белков, кодируемых мтДНК, ND6 в сыворотке был повышен при активном васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами, а концентрация ND6 отрицательно коррелировала с процентом нормальных клубочков в биоптатах почек [66]. Эти исследования показали, что сывороточная мтДНК отражает иммунный воспалительный статус и повреждение почек.

Нажмите здесь, чтобы узнатьчто такое цистанхе
Опосредованное мтДНК сыворотки иммунное отторжение определяет эффективность трансплантации почки. Чем выше уровень мтДНК в сыворотке крови донора почки, тем больше вероятность того, что реципиент почечного трансплантата испытает отторжение, опосредованное антителами. Следовательно, мтДНК донорской сыворотки можно использовать в качестве прогностического маркера опосредованного антителами отторжения и подтвержденной оценки донорских органов [67]. Соответственно, мтДНК донорской плазмы была независимым фактором риска задержки функции трансплантата (ЗФТ) у реципиентов почки, что было ценно при оценке органов [68].
2. мтДНК в моче
мтДНК в моче можно использовать в качестве индикатора для оценки функции почек. Острое повышение уровня мтДНК в моче при чрескожной транслюминальной почечной ангиопластике отражает повреждение митохондрий почек и, таким образом, препятствует восстановлению почек [69]. У пациентов с сепсисом повышенные уровни мтДНК в моче были связаны с дисфункцией митохондрий и повреждением почек, что свидетельствует о том, что сепсис вызывает повреждение митохондрий почек. Таким образом, мтДНК в моче можно считать ценным биомаркером для определения развития ОПП и митохондриально-направленной терапии после сепсис-индуцированного ОПП [70]. По сравнению со здоровым контролем экспрессия STING в почках была увеличена, а уровни мтДНК в моче были повышены у пациентов с болезнью минимальных изменений (БМИ), что можно было бы использовать в качестве ценного прогностического маркера при БМИ [71]. Уровни мтДНК в моче были значительно повышены как у пациентов с диабетом, так и у мышей, что отрицательно коррелировало со скоростью клубочковой фильтрации и положительно коррелировало с интерстициальным фиброзом [63,72]. мтДНК также была легко обнаружена в супернатанте мочи при недиабетической ХБП, и ее уровень коррелировал со скоростью снижения почечной функции и предсказывал риск повышения уровня креатинина в сыворотке и потребность в диализе у пациентов с ХБП [73]. Низкий уровень мтДНК в моче значительно коррелировал с благоприятными почечными исходами через 6 месяцев наблюдения, что указывает на новую прогностическую роль мтДНК для почечных исходов у пациентов с ХБП [74]. У пациентов с реноваскулярной гипертензией повышенное количество копий мтДНК в моче коррелировало с митохондриальной дисфункцией и повреждением почек, включая повышение уровня липокалина, ассоциированного с желатиназой нейтрофилов в моче, уровни молекулярного -1 повреждения почек (KIM-1) и снижение расчетного клубочкового фильтрация [75,76]. Более высокое число копий мтДНК в моче и более высокие среднегодовые темпы снижения расчетной скорости клубочковой фильтрации (рСКФ) были обнаружены у пациентов с небольшими гломерулярными аномалиями и IgA-нефропатией (IgAN), а повреждение митохондрий могло быть до патологических изменений и повышенной протеинурии [77,78]. Уровень мтДНК в моче был повышен у пациентов с васкулитом, ассоциированным с антинейтрофильными цитоплазматическими аутоантителами (ANCA-AAV), страдающих нарушением функции почек, и его уровень коррелировал с тяжестью почечного повреждения и патологической нейтрофильной инфильтрацией [79]. Уровень мтДНК в моче коррелировал со временем холодовой ишемии и функцией почек у реципиентов почечного трансплантата, что было связано с функцией почечного аллотрансплантата и диагнозом DGF после трансплантации почки [80]. Уровень мтДНК в моче был значительно выше у пациентов с острым отторжением и DGF, что может быть прогностическим фактором краткосрочной посттрансплантационной функции почек [81]. В совокупности вышеуказанные исследования показывают, что мтДНК в моче тесно связана с изменениями почечной функции при различных заболеваниях почек, а высокий уровень мтДНК в моче является неблагоприятным фактором.

Цистанхе трубчатая
Повреждение мтДНК при заболеваниях почек
1. Нарушение репликации мтДНК
мтДНК реплицируется в культивируемых клетках почек по асинхронному механизму [82]. Снижение числа копий мтДНК в образцах крови было связано с аномальными уровнями креатинина в сыворотке крови, что указывало на нарушение функции почек [83]. Во время репликации мтДНК роль mtSSB1 заключается в защите смещенной одноцепочечной ДНК от повреждения, предотвращении образования вторичных структур ДНК и связывании несоответствующих синтеза ДНК и катаболических ферментов. Густафсон и др. сообщили о случае молодого пациента с ХБП, имеющего мутацию mtSSB1 (p.E27K), сопровождающуюся одной крупномасштабной делецией мтДНК [84]. Содержание мтДНК в почках также было значительно снижено у пациентов с мутацией SSBP1 (p.R107Q) с нарушением OXPHOS и недостаточностью функции почек, требующей трансплантации [85]. За исключением мтДНК отделов головного мозга, мтДНК почек оказалась наиболее уязвимой к накоплению возрастных повреждений, а число копий мтДНК в почках старых крыс было значительно увеличено [86]. Кроме того, уровни мтДНК были значительно выше в проксимальных и дистальных канальцах, чем в эпителии клубочков и собирательных трубочек почек. С возрастом содержание мтДНК в почечных канальцах снижалось, что согласовывалось с постепенным снижением функции почек и могло быть устранено ограничением калорийности [87]. В целом репликация мтДНК является биомаркером митохондриальной функции, что связано с повышенной смертностью и заболеваемостью при возрастных заболеваниях [88].
Недавние исследования показали, что нарушение репликации мтДНК способствует ОПП. Репликация и содержание мтДНК снижались при усилении митофагии в почках, что способствовало возникновению ОПП и увеличению смертности у крыс после трансплантации печени [89]. Количество копий мтДНК было снижено в моделях почечного фиброза, включая одностороннюю обструкцию мочеточника (UUO) и IRI, сопровождающуюся митохондриальной дисфункцией и окислительным стрессом [90]. Индуцируемый гипоксией фактор -1 (HIF-1)-BCL2/аденовирус E1B 19 кДа, взаимодействующий с белком 3 (BNIP3), опосредованная митофагией, регулирует количество копий мтДНК и продукцию АФК и ингибирует клеточный апоптоз в клетках почечных канальцев модели IRI [91].
Существуют различные причины ХБП с аномальной репликацией мтДНК. Сниженное число копий мтДНК в мононуклеарных клетках периферической крови больных МГБ предсказывало неблагоприятные клинические исходы [92]. Соответственно, количество копий мтДНК уменьшалось в почках мышей с диабетом, что сопровождалось подавлением экспрессии TFAM и продукции АТФ [93]. Точно так же наше предыдущее исследование показало, что нарушение репликации мтДНК в подоцитах способствует повреждению почек при диабетической болезни почек (ДБП) [94]. Делеция мтДНК также усугубляла повреждение и истощение подоцитов, что было вовлечено в патогенез фокально-сегментарного гломерулосклероза (ФСГС) [95]. Снижение содержания мтДНК было основной причиной снижения OXPHOS при хромофобном раке почки (ХПКР) [96]. Последнее исследование показало, что дефекты репликации мтДНК приводят к формированию линейной делеции мтДНК, которая запускает иммунный ответ и приводит к прогрессирующему заболеванию почек у стареющих животных [97].

Экстракт цистанхе
2. Мутации мтДНК
Почка — это не только орган с высокой репликацией мтДНК. Он также содержит несколько сайтов мутаций мтДНК, которые могут быть мутированы [98]. Следствием мутаций мтДНК является митохондриальная дисфункция. Мутации мтДНК обычно вызывают системные заболевания, которые также могут быть связаны с прогрессированием ОПП и ХБП [28]. Заболевания почек, вызванные мутациями мтДНК в разных локусах, обобщены в таблице 1.
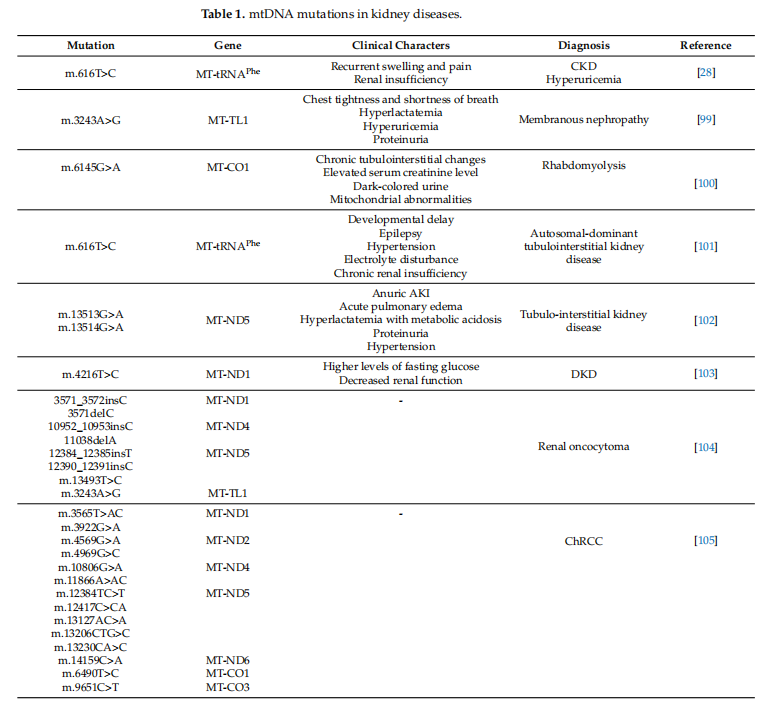
An adenine to guanine substitution at nucleotide 3243 of the mtDNA (m.3243A>G), which affects the mitochondrial MT-TL1 gene, has been shown to cause mitochondrial encephalomyopathy, lactic acidosis, and stroke-like episodes (MELAS) syndrome. The most striking characteristics of renal biopsy were FSGS and arteriolar hyaline thickening [116]. Cai et al. recently reported that a patient with m.3243A>Мутация G была диагностирована с мембранозной нефропатией, а ОПП, осложненное гиперурикемией, может быть связано с мутациями мтДНК [99].
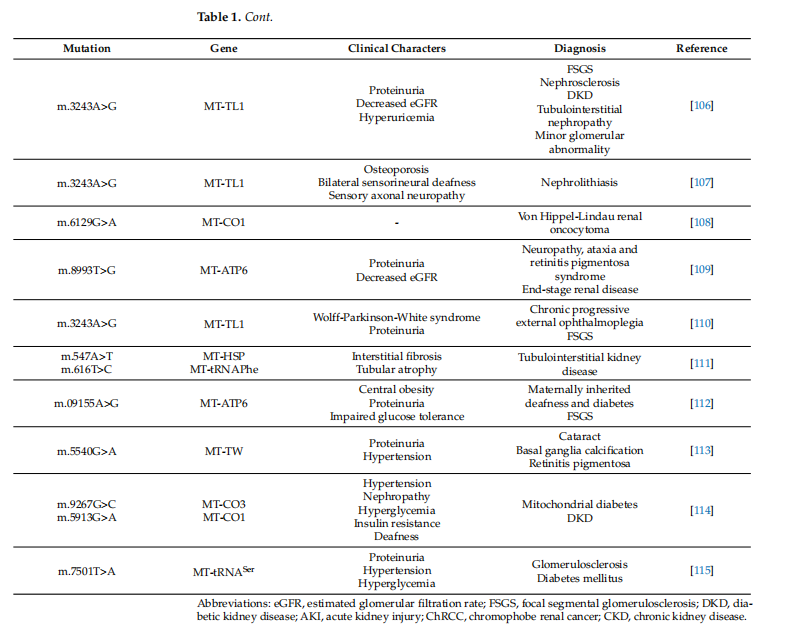
A novel heteroplasmic nonsense mtDNA mutation m.6145G>A in the mitochondrial cytochrome c oxidase subunit I (MTCO1) was also identified in a patient who exhibited mitochondrial abnormalities, chronic tubulointerstitial changes and recurrent episodes of rhabdomyolysis [100]. Mitochondrial tubulointerstitial nephropathy (MITKD) is a tubulointerstitial nephropathy caused by mutations in mtDNA. m.616T>C is one of the mutations that lead to MITKD, the main symptoms of which are chronic renal insufficiency and Epilepsia [101]. It has also been reported that two mt-ND5 pathogenic variants m.13513G>A and m.13514A>G caused mitochondrial dysfunction in tubulointerstitial kidney disease [102]. Aristolochic acid elevated the levels of mutagenic 8-oxo-20 -deoxyguanosine and 7-(deoxyadenosine-N6-yl)-aristo lactam adduct on mtDNA isolated from human HEK293 cells, which shed light on a potentially important causative role of mtDNA mutations and mitochondrial dysfunction in the etiology of aristolochic acid nephropathy [117]. Patients with type 2 diabetes diagnosed with the m.4216T>C mtDNA mutation are more likely to have poor glycemic control, which triggers the progression of DKD [103]. However, an mtDNA mutation m.8344A>G в митохондриальном гене tRNALys, вызывающем миоклоническую эпилепсию с синдромом рваных красных волокон (MERRF), не влияет на число копий мтДНК и функцию почек [118].
Комплексное ресеквенирование мтДНК было применено для обнаружения мутаций в клинических образцах, и несколько видов опухолевых тканей были исследованы на наличие мутаций мтДНК, включая почечно-клеточный рак (ПКР) [119]. Мутационный анализ мтДНК выявил мутации в гене субъединицы I митохондриального комплекса ND1, ND5 и ND6, что способствует дефициту дыхательной цепи и возникновению онкоцитомы почек [104]. ХПКР является подтипом ПКР, который сопровождается высокой частотой мутаций мтДНК [120]. Анализ секвенирования мтДНК показал, что мутации мтДНК приводят к функциональной недостаточности субъединиц НАДН-дегидрогеназы, что в дальнейшем способствует трансформации метаболического паттерна при ХПКР [105].
Стандартизированный цистанхе
3. Утечка мтДНК
Почка – это орган, богатый мтДНК. При стимуляции почек вредными факторами мтДНК может высвобождаться из митохондриального матрикса в цитоплазму. Вызванная цисплатином утечка мтДНК в цитозоль, вероятно, через поры BAX в наружной мембране митохондрий в почечных канальцах с последующей активацией пути cGAS-STING, вызывая тем самым воспаление и прогрессирование ОПП [121]. Взаимодействующая с рецептором протеинкиназа 3 транслоцируется в митохондрии и взаимодействует с митофилином, что приводит к повышенному высвобождению мтДНК и активации пути cGAS-STING-p65 при ИРИ почек [122]. У мышей с канальцево-специфическим нокаутом TFAM аберрантная упаковка мтДНК приводила к цитозольной транслокации, которая дополнительно активировала цитозольный путь cGAS-STING и привлекала цитокины и иммунные клетки для усугубления фиброза почек [123]. При ДБП подавление супероксиддисмутазы 2 опосредует митохондриальную дисфункцию и утечку мтДНК, что может активировать TLR9 в макрофагах [124]. Таким образом, утечка мтДНК может быть сопутствующим феноменом повреждения почек и опосредовать развитие множественных воспалительных реакций.
4. Метилирование мтДНК
Текущие исследования метилирования мтДНК в почках до сих пор остаются слепым пятном. Сообщалось только об одном исследовании корреляции между метастазированием опухоли в почки и метилированием мтДНК. Показано, что по сравнению с первичными клетками ПКР область D-петли мтДНК была заметно гиперметилирована в клетках метастатического ПКР в кости, что обеспечивает прямую связь между гиперметилированием мтДНК в клетках ПКР и ростом опухоли при метастазах в кости [125]. Из-за технологических ограничений и проблем с затратами на обнаружение метилирования мтДНК прогресс исследований в этой области относительно низок. При постоянном внимании и приверженности исследованиям в этой области роль метилирования мтДНК в заболеваниях почек будет постоянно изучаться.
Цистанхе добавка
Фармакологическое вмешательство при повреждении мтДНК при заболеваниях почек
Как обсуждалось в предыдущем разделе, содержание и целостность мтДНК в почках нарушается при этиологии различных заболеваний почек. Повреждение мтДНК может напрямую влиять на функцию митохондрий. Следовательно, целенаправленные вмешательства против повреждения мтДНК могут иметь терапевтический эффект при заболеваниях почек.
В настоящее время для вмешательства в повреждение почечной мтДНК применяется широкий спектр агентов, как показано в таблице 2. Мы обобщили фармакологические механизмы этих агентов и обнаружили, что большинство из них облегчают повреждение почек и клеточный апоптоз за счет улучшения митохондриальных функций, таких как увеличение мтДНК. содержание, гамма-коактиватор рецептора, активируемого пролифератором пероксисом -1 (PGC-1), и экспрессия рецептора, активируемого пролифератором пероксисом (PPAR), которые способствуют митохондриальному OXPHOS для облегчения снабжения энергией и снижения окислительного стресса, продукции АФК, и воспаление. Существует также несколько терапевтических агентов, таких как L-карнитин и сакубитрил/валсартан, которые ослабляют воспалительную реакцию, активируемую утечкой мтДНК, путем подавления связанных с воспалением путей, таких как сигнальные пути TLR9 и cGAS-STING [124, 126].

Сообщалось также о нескольких других альтернативных методах лечения. Например, внеклеточные везикулы (ВВ), полученные из мезенхимальных стволовых клеток (МСК), содержат функциональные митохондриальные компоненты, такие как мтДНК, митохондриальные белки и связанные с энергией белки из цикла трикарбоновых кислот [135]. Опосредованный MSC-EV перенос мРНК TFAM восстанавливал экспрессию TFAM, делецию мтДНК и дефекты OXPHOS в клетках почечных канальцев при ОПП [136]. Последние исследования показывают, что митохондриальная трансплантация может быть новым методом лечения митохондриальных заболеваний. Прямое экзогенное добавление митохондрий может заменить поврежденную мтДНК, восстановить функцию митохондрий и ингибировать окислительный стресс, тем самым уменьшая апоптоз [137,138]. Более того, митохондриальная заместительная терапия может применяться при наследственных заболеваниях, вызванных мутациями в мтДНК [139].
Выводы и перспективы на будущее
Интактная мтДНК тесно связана с функцией митохондрий. В мтДНК отсутствует сложная система самовосстановления, и она восприимчива к множеству внешних и внутренних факторов, включая лекарства, инфекции, нарушения иммунной системы, гипертонию, диабет и старение. Все эти причины могут приводить к повреждению мтДНК, что еще больше усиливает митохондриальную дисфункцию, проявляющуюся в дефектах ЭТЦ, снижении OXPHOS, окислительном стрессе и воспалительной реакции, таким образом участвуя в процессе повреждения почек. Поэтому крайне важно изучить роль повреждения мтДНК в заболевании почек.
В этом обзоре мы тщательно изучили распространенные типы повреждений мтДНК, включая нарушение репликации мтДНК, мутации мтДНК, утечку мтДНК и метилирование мтДНК. Всесторонне описаны механизмы этих типов повреждений, а также подробно обобщены исследования, связанные с повреждением мтДНК при заболеваниях почек. Было обнаружено, что повреждение мтДНК играет важную роль в заболеваниях почек, а уровни мтДНК в периферической плазме и моче указывают на маркерную роль в заболеваниях почек. Фармакологическое лечение или экзогенная трансплантация мтДНК могут улучшать состояние поврежденной мтДНК, восстанавливать функцию митохондрий или напрямую ингибировать воспалительную реакцию, индуцированную мтДНК, тем самым обеспечивая теоретическую основу и новые возможности для лечения заболеваний почек. В заключение, повреждение мтДНК служит ключевым биомаркером заболеваний почек.
Рекомендации
55. Кушен, Южная Каролина; Риччи, Калифорния; Брэдшоу, Дж. Л.; Зильцер, Т .; Благословение, А .; Сан, Дж.; Чжоу, З .; Скроггинс, С.М.; Сантильян, МК; Сантильян, Д.А.; и другие. Снижение материнской циркулирующей внеклеточной митохондриальной ДНК связано с развитием преэклампсии. Варенье. Сердечный доц. 2022, 11, e21726. [Перекрестная ссылка]
56. Вэй Р.; Ни, Ю .; Базли, П.; Гранди, С.; Ван, Дж.; Список; Хазен, С.Л.; Уилсон, ТВ; ЛаФрамбуаз, Т. Содержание митохондриальной ДНК связано с фенотипами пациентов с сердечно-сосудистыми заболеваниями. Варенье. Сердечный доц. 2021, 10, e18776. [Перекрестная ссылка]
57. Чжун, В.; Рао, З .; Рао, Дж.; Вешать.; Ван, П.; Цзян, Т .; Пан, X .; Чжоу, С .; Чжоу, Х .; Ван, X. Старение усугубляет ишемию печени и реперфузионное повреждение, способствуя STING-опосредованной активации NLRP3 в макрофагах. Стареющая клетка 2020, 19, e13186. [Перекрестная ссылка]
58. Гонсалес-Фрейре, М.; Мур, Аризона; Петерсон, Калифорния; Космак, К.; Макдермотт, М.М.; Суфит, Р.Л.; Гуральник, Дж. М.; Полонский, Т .; Тиан, Л .; Киббе, МР; и другие. Ассоциации заболевания периферических артерий с гетероплазмией митохондриальной ДНК скелетных мышц голени. Варенье. Сердечный доц. 2020, 9, e15197. [Перекрестная ссылка]
59. Хомолова, Ю.; Яновикова, Л.; Конекна, Б.; Влкова, Б.; Селек, П.; Тотова, Л.; Бабикова, Дж. Концентрация внеклеточной ДНК в плазме крови при остром повреждении почек. Диагностика 2020, 10, 152. [CrossRef]
60. Ву, Дж.; Рен, Дж.; Лю, В.; Ху, В.; Ву, Х .; Ван, Г.; Хонг, З .; Рен, Х .; Ли, Дж. Влияние изменений уровней молекулярных паттернов, связанных с повреждением, после непрерывной вено-венозной гемофильтрационной терапии на исходы у пациентов с острым повреждением почек с сепсисом. Передний. Иммунол. 2018, 9, 3052. [Перекрестная ссылка]
61. Янцушка, А.; Потокарова, А.; Ковальчикова, А.Г.; Подрацкая, Л.; Бабикова, Дж.; Селек, П.; Тотова, Л. Динамика внеклеточной ДНК плазмы и мочи при остром повреждении почек. Междунар. Дж. Мол. науч. 2022, 23, 3402. [CrossRef] [PubMed]
62. Он, В.Дж.; Ли, К .; Хуанг, З .; Генг, С .; Рао, В.С.; Келли, Теннесси; Хэмм, Л. Л.; Граммы, Мэн; Аркинг, Делавэр; Аппель, ЖЖ; и другие. Ассоциация числа копий митохондриальной ДНК с риском прогрессирования заболевания почек. клин. Варенье. соц. Нефрол. 2022, 17, 966–975. [Перекрестная ссылка] [PubMed]
63. Цао, Х.; Ву, Дж.; Луо, Дж .; Чен, X .; Ян, Дж .; Fang, L. Мочевая митохондриальная ДНК: потенциальный ранний биомаркер диабетической нефропатии. Диабет метаб. Рез. Ред. 2019, 35, e3131. [Перекрестная ссылка] [PubMed]
64. Сзето, CC; Лай, КБ; Чоу, км; Кван, Британская Колумбия; Ченг, премьер-министр; Квонг, Фольксваген; Чой, А.С.; Люнг, CB; Ли, П.К. Уровень митохондриальной ДНК в плазме является прогностическим маркером у пациентов на перитонеальном диализе. Почечный пресс крови Res. 2016, 41, 402–412. [Перекрестная ссылка] [PubMed]
65. Фан З.; Го, Ю .; Zhong, XY Циркулирующая бесклеточная митохондриальная ДНК: потенциальный биомаркер саркопении у пациентов, находящихся на поддерживающем гемодиализе. Мед. науч. Монит. 2022, 28, e934679.
66. Тиан, С.Л.; Бай, X .; Сюй, ПК; Чен, Т .; Гао, С .; Ху, Си; Вэй, Л.; Цзя, JY; Ян, Т.К. Циркулирующая никотинамидадениндинуклеотидная цепь убихиноноксидоредуктазы 6 связана с активностью заболевания васкулитом, ассоциированным с антинейтрофильными цитоплазматическими антителами. клин. Чим. Acta 2020, 511, 125–131. [Перекрестная ссылка]
67. Хан, Ф.; Солнце, В.; Хуанг, З .; Ли, Х .; Ма, М .; Ляо, Т .; Луо, З .; Чжэн, Л .; Чжан, Н .; Чен, Н .; и другие. Митохондриальная ДНК донорской плазмы связана с опосредованным антителами отторжением у реципиентов почечного аллотрансплантата. Старение (Олбани, штат Нью-Йорк) 2021, 13, 8440–8453. [Перекрестная ссылка]
68. Хан, Ф.; Ван, С .; Солнце, В.; Чен, Н .; Ли, Х .; Чжэн, Л .; Чжан, Н .; Хуанг, З .; Хонг, Л.; Sun, Q. Митохондриальная ДНК донорской плазмы коррелирует с функцией посттрансплантационного почечного аллотрансплантата. Трансплантация 2019, 103, 2347–2358. [Перекрестная ссылка]
69. Эйрин, А.; Херрманн, С.М.; Саад, А .; Абумоавад, А .; Тан, Х .; Лерман, А .; Текстор, Южная Каролина; Лерман, Л.О. Число копий митохондриальной ДНК мочи определяет повреждение митохондрий почек у пациентов с реноваскулярной гипертензией, перенесших реваскуляризацию почек: экспериментальное исследование. Акта Физиол. (Оксф) 2019, 226, e13267. [Перекрестная ссылка]
70. Ху, В.; Рен, Дж.; Рен, Х .; Ву, Дж.; Ву, Х .; Лю, С .; Ван, Г.; Гу, Г .; Го, К .; Ли, Дж. Митохондриальная ДНК мочи определяет дисфункцию почек и митохондриальное повреждение при остром повреждении почек, вызванном сепсисом. Оксид Мед. Сотовый Лонгев. 2018, 2018, 8074936. [Перекрестная ссылка]
71. Ю. Б. С.; Мун, А .; Ли, К. Х.; О, ЮС; Парк, штат Мэн; Чой, SJ; Ким, Дж. К. Болезнь с минимальными изменениями связана с повреждением митохондрий и активацией пути STING. Дж. Клин. Мед. 2022, 11, 577. [CrossRef] [PubMed]
72. Вэй, П.З.; Кван, Британская Колумбия; Чоу, км; Ченг, премьер-министр; Лук, CC; Ли, ПК; Szeto, CC Уровень митохондриальной ДНК в моче является индикатором внутрипочечного истощения митохондрий и почечного рубцевания при диабетической нефропатии. Нефрол. Набирать номер. Транспл. 2018, 33, 784–788. [Перекрестная ссылка] [PubMed]
73. Вэй, П.З.; Кван, Британская Колумбия; Чоу, км; Ченг, премьер-министр; Лук, CC; Лай, КБ; Ли, ПК; Szeto, CC Уровень митохондриальной ДНК в моче при недиабетических хронических заболеваниях почек. клин. Чим. Acta 2018, 484, 36–39. [Перекрестная ссылка] [PubMed]
74. Чанг, CC; Чиу, ПФ; Ву, CL; Куо, CL; Хуанг, CS; Лю, CS; Huang, CH Бесклеточная митохондриальная и ядерная дезоксирибонуклеиновая кислота в моче коррелирует с прогнозом хронических заболеваний почек. БМК Нефрол. 2019, 20, 391. [Перекрестная ссылка]
75. Эйрин, А.; Саад, А .; Тан, Х .; Херрманн, С.М.; Вуллард, младший; Лерман, А .; Текстор, Южная Каролина; Лерман, Л.О. Число копий митохондриальной ДНК мочи определяет хроническое повреждение почек у пациентов с гипертонической болезнью. Гипертония 2016, 68, 401–410. [Перекрестная ссылка]
76. Эйрин, А.; Саад, А .; Вуллард, младший; Юнкос, Луизиана; Калхун, Д.А.; Тан, Х .; Лерман, А .; Текстор, Южная Каролина; Лерман, Л.О. Гломерулярная гиперфильтрация у тучных афроамериканских пациентов с гипертонической болезнью связана с повышенным числом копий митохондриальной ДНК в моче. Являюсь. Дж. Гипертензии. 2017, 30, 1112–1119. [Перекрестная ссылка]
77. Ю. Б. С.; Чо, Нью-Джерси; Парк, С.; Ким, Х .; Гил, Х.В.; Ли, Эй; Квон, С.Х.; Чон, JS; Но, Х .; Хан, округ Колумбия; и другие. Незначительные гломерулярные аномалии связаны с долгосрочным ухудшением функции почек и повреждением митохондрий. Дж. Клин. Мед. 2019, 9, 33. [Перекрестная ссылка]
78. Ю. Б. С.; Чо, Нью-Джерси; Парк, С.; Ким, Х .; Чой, SJ; Ким, Дж. К.; Хван, SD; Гил, Х.В.; Ли, Эй; Чон, JS; и другие. IgA-нефропатия связана с повышенным числом копий митохондриальной ДНК в моче. науч. Отчет 2019, 9, 16068. [CrossRef]
79. Ву, С.Дж.; Ян, X .; Сюй, ПК; Чен, Т .; Гао, С .; Ху, Си; Вэй, Л.; Ян, Т.К. Митохондриальная ДНК мочи является полезным биомаркером для оценки повреждения почек при васкулите, ассоциированном с антинейтрофильными цитоплазматическими антителами. клин. Чим. Acta 2020, 502, 263–268. [Перекрестная ссылка]
80. Янсен, М.; Пульскенс, В.; Уил, М .; Классен, Н.; Ньювенхейзен, Г.; Стандарт, Д.; Хау, см; Ньюланд, Р .; Флоркин, С .; Бемельман, Ф.Дж.; и другие. Митохондриальная ДНК мочи связана с задержкой функции трансплантата после трансплантации почки. Нефрол. Набирать номер. Транспл. 2020, 35, 1320–1327. [Перекрестная ссылка]
81. Ким, К.; Мун, Х .; Ли, Ю. Х.; Сео, JW; Ким, Ю. Г.; Луна, JY; Ким, Дж. С.; Чон, К.Х.; Ли, ТВ; Им, К.Г.; и другие. Клиническая значимость внеклеточной митохондриальной ДНК в раннем послеоперационном периоде у реципиентов почечного трансплантата. науч. Отчет 2019, 9, 18607. [CrossRef] [PubMed]
82. Герберс, Э.; Кекалайнен, Нью-Джерси; Хангас, А .; Похёисмяки, Дж. Л.; Гоффарт, С. Тканеспецифические различия в поддержании и экспрессии митохондриальной ДНК. Митохондрия 2019, 44, 85–92. [Перекрестная ссылка] [PubMed]
83. Лоншам, Р. Дж.; Ян, Си; Кастеллани, Калифорния; Ши, В .; Лейн, Дж.; Гроув, МЛ; Барц, ТМ; Сарновски, К.; Лю, К.; Берроуз, К.; и другие. Полногеномный анализ числа копий митохондриальной ДНК выявляет локусы, участвующие в метаболизме нуклеотидов, активации тромбоцитов и пролиферации мегакариоцитов. Гум. Жене. 2022, 141, 127–146. [Перекрестная ссылка]
84. Густафсон, Массачусетс; Маккормик, Э.М.; Перера, Л.; Лонгли, М.Дж.; Бай, Р .; Конг, Дж.; Дулик, М.; Шен, Л.; Гольдштейн, AC; Маккормак, SE; и другие. Митохондриальная одноцепочечная ДНК-связывающий белок, новая мутация de novo SSBP1 у ребенка с одиночной крупномасштабной делецией мтДНК (SLSMD), клинически проявляющаяся синдромами Пирсона, Кернса-Сейра и Ли. PLoS ONE 2019, 14, e221829. [Перекрестная ссылка] [PubMed]
85. Дел, Д.В.; Улла, Ф .; Ди Мео, И.; Магини, П .; Гусич, М.; Мареска, А .; Капорали, Л.; Паломбо, Ф.; Тальявини, Ф .; Боуг, Э. Х.; и другие. Мутации SSBP1 вызывают истощение мтДНК, лежащее в основе сложной атрофии зрительного нерва. Дж. Клин. расследование 2020, 130, 108–125.
86. Гуреев, А.П.; Андрианова, Н.В.; Певзнер, И.Б.; Зорова, Л.Д.; Чернышова, Е.В.; Садовникова И.С.; Чистяков Д.В.; Попков, В.А.; Семенович, Д.С.; Бабенко, В.А.; и другие. Диетическое ограничение модулирует повреждение митохондриальной ДНК и профиль оксилипина у старых крыс. FEBS J. 2022, 289, 5697–5713. [Перекрестная ссылка]
87. Чен, Дж.; Чжэн, Q .; Пайффер, Л.Б.; Хикс, Дж. Л.; Хаффнер, MC; Розенберг, Аризона; Леви, М.; Ван, ХХ; Озбек, Б .; Баэна-Дель, виджей; и другие. Атлас митохондриальной ДНК in situ в тканях млекопитающих показывает ее высокое содержание в стволовых и пролиферативных отделах. Являюсь. Дж. Патол. 2020, 190, 1565–1579. [Перекрестная ссылка]
88. Фукунага, Х. Число копий митохондриальной ДНК и генетическое происхождение здоровья и болезней (DOHaD). Междунар. Дж. Мол. науч. 2021, 22, 6634. [Перекрестная ссылка]
89. Лю, В.; Кришнасами, Ю.; Рехман, Х .; Лемастерс, Дж. Дж.; Шнельманн, Р. Г.; Чжун, З. Нарушенный почечный митохондриальный гомеостаз после трансплантации печени у крыс. PLoS ONE 2015, 10, e140906. [Перекрестная ссылка]
90. Ляо, X.; Ур., Х.; Чжан, Ю .; Хан, Ю.; Ли, Дж.; Цзэн, Дж.; Тан, Д.; Мэн, Дж .; Юань, X .; Пэн, З .; и другие. Фторофенидон ингибирует UUO/IRI-индуцированный фиброз почек, уменьшая повреждение митохондрий. Оксид Мед. Сотовый Лонгев. 2022, 2022, 2453617. [Перекрестная ссылка]
91. Фу, З.Дж.; Ван, ZY; Сюй, Л.; Чен, XH; Ли, ХХ; Ляо, Вт; Ма, Гонконг; Цзян, доктор медицины; Сюй, ТТ; Сюй, Дж.; и другие. Опосредованная HIF-1альфа-BNIP3- митофагия в канальцевых клетках защищает от почечной ишемии/реперфузионного повреждения. Redox Biol 2020, 36, 101671. [CrossRef] [PubMed]
92. Рао, М.; Ли, Л .; Демелло, К.; Го, Д .; Джабер, Б.Л.; Перейра, Б.Дж.; Балакришнан, В.С. Повреждение митохондриальной ДНК и смертность у пациентов, находящихся на гемодиализе. Варенье. соц. Нефрол. 2009, 20, 189–196. [Перекрестная ссылка] [PubMed]
93. Ахтар, С.; Siragy, HM Прорениновый рецептор подавляет митохондриальный биогенез и функцию через путь AMPK/SIRT-1/PGC-1альфа в диабетической почке. PLoS ONE 2019, 14, e225728. [Перекрестная ссылка] [PubMed]
94. Фэн, Дж.; Чен, З .; Может.; Ян, X .; Чжу, З .; Чжан, З .; Ху, Дж.; Лян, В .; Дин, Г. AKAP1 способствует нарушению репликации мтДНК и митохондриальной дисфункции в подоцитах диабетической болезни почек. Междунар. Журнал биологических наук. 2022, 10, 4026–4042. [Перекрестная ссылка]
95. Канеко, С.; Усуи, Дж.; Хагивара, М .; Симидзу, Т .; Исии, Р .; Такахаши-Кобаяши, М.; Кагеяма, М .; Накада, К .; Хаяси, Дж.И.; Ямагата, К. Зависимые от делеции митохондриальной ДНК повреждения подоцитов у мышей Mito-miceDelta, мышиной модели митохондриального заболевания. Эксп. Аним. 2022, 71, 14–21. [Перекрестная ссылка]
96. Сяо Ю.; Клима, Р.; Буш, Дж.; Рабиен, А .; Килич, Э .; Вильегас, С.Л.; Тиммерманн, Б.; Аттимонелли, М.; Юнг, К.; Мейерхофер, Д. Снижение содержания митохондриальной ДНК приводит к нарушению регуляции OXPHOS при хромофобной почечно-клеточной карциноме. Рак Рез. 2020, 80, 3830–3840. [Перекрестная ссылка]
97. Миленкович Д.; Санс-Морено, А .; Кальзада-Вак, Дж.; Ратколб, Б.; Вероника, АО; Герлини, Р.; Агилар-Пиментель, А .; Мизик, Дж.; Симард, мл.; Вольф, Э .; и другие. У мышей, лишенных митохондриальной экзонуклеазы MGME1, развивается воспалительное заболевание почек с гломерулярной дисфункцией. Генетика PLoS. 2022, 18, e1010190. [Перекрестная ссылка]
98. Сэмюэлс, округ Колумбия; Ли, К .; Ли, Б.; Песня, З .; Торстенсон, Э.; Бойд, CH; Рокас, А .; Торнтон-Уэллс, Т.А.; Мур, Дж. Х.; Хьюз, ТМ; и другие. Рекуррентные тканеспецифические мутации мтДНК часто встречаются у людей. Генетика PLoS. 2013, 9, e1003929. [Перекрестная ссылка]
99. Кай, М.; Ю, К.; Бао, Дж. Случай митохондриальной миопатии с мембранозной нефропатией. БМК Нефрол. 2022, 23, 87. [Перекрестная ссылка]
100. Фервенза, ФК; Гаврилова Р.Х.; Наср, С.Х.; Иразабал, М.В.; Нат, К.А. ХЗП из-за новой мутации митохондриальной ДНК: клинический случай. Являюсь. Дж. Почки Дис. 2019, 73, 273–277. [Перекрестная ссылка]
101. Lorenz, R.; Ahting, U.; Betzler, C.; Heimering, S.; Borggrafe, I.; Lange-Sperandio, B. Homoplasmy of the Mitochondrial DNA Mutation m.616T>C Приводит к митохондриальной тубулоинтерстициальной болезни почек и энцефалопатии. Нефрон 2020, 144, 156–160. [Перекрестная ссылка] [PubMed]
102. Бакис, Х.; Тримуль, А .; Верморель, А .; Редоннет, И.; Гойзе, К.; Булестро, Р.; Лакомб, Д.; Комб, К.; Мартин-Негриер, мл.; Риготье, К. Тубулоинтерстициальная нефропатия с началом во взрослом возрасте при фенотипах, связанных с MT-ND5-. клин. Жене. 2020, 97, 628–633. [Перекрестная ссылка] [PubMed]
103. Диас-Моралес, Н.; Лопес-Доменек, С.; Яннантуони, Ф.; Лопес-Гальярдо, Э.; Сола, Э.; Мориллас, К.; Роча, М .; Руис-Песини, Э.; Victor, VM Гаплогруппа JT митохондриальной ДНК связана с нарушением гликемического контроля и функции почек у пациентов с диабетом 2 типа. Дж. Клин. Мед. 2018, 7, 220. [CrossRef] [PubMed]
104. Майр, Дж. А.; Мейерхофер, Д.; Циммерманн, Ф .; Файхтингер, Р .; Коглер, К.; Рачек, М .; Шмеллер, Н.; Сперл, В .; Кофлер, Б. Потеря комплекса I из-за мутаций митохондриальной ДНК при онкоцитоме почек. клин. Рак Рез. 2008, 14, 2270–2275. [Перекрестная ссылка]
105. Дэвис, CF; Рикеттс, СиДжей; Ван, М .; Ян, Л .; Черняк, AD; Шен, Х .; Бухай, К.; Канг, Х .; Ким, Южная Каролина; Фэйи, CC; и другие. Соматический геномный ландшафт хромофобной почечно-клеточной карциномы. Раковая клетка 2014, 26, 319–330. [Перекрестная ссылка]
106. Имасава, Т.; Хирано, Д.; Нозу, К .; Китамура, Х .; Хаттори, М .; Сугияма, Х .; Сато, Х .; Мураяма, К. Клиникопатологические особенности митохондриальной нефропатии. почки инт. 2022, 7, 580–590. [Перекрестная ссылка]
107. Bargagli, M.; Primiano, G.; Primiano, A.; Gervasoni, J.; Naticchia, A.; Servidei, S.; Gambaro, G.; Ferraro, P.M. Recurrent kidney stones in a family with a mitochondrial disorder due to the m.3243A>Мутация G. Мочекаменная болезнь 2019, 47, 489–492. [Перекрестная ссылка]
108. Де Луиза, М.; Гварньери, В.; Чеккарелли, К.; Д'Агрума, Л.; Порчелли, AM; Гаспар, Г. Бессмысленная мутация митохондриальной ДНК, связанная с дисфункцией HIF1-альфа при онкоцитоме почки фон Хиппеля-Линдау. Оксид Мед. Сотовый Лонгев. 2019, 2019, 8069583. [Перекрестная ссылка]
109. Лемуан, С.; Панайе, М.; Рабейрин, М.; Эрразурис-Серда, Э.; Муссон, DCB; Петио, П.; Джульярд, Л.; Гебре-Эгзиабхер, Ф. Вовлечение почек в невропатию, атаксию, синдром пигментного ретинита (NARP): клинический случай. Являюсь. Дж. Почки Дис. 2018, 71, 754–757. [Перекрестная ссылка]
110. Наруми, К.; Мисима, Э .; Акияма, Ю.; Мацухаши, Т .; Накамичи, Т .; Кису, К .; Нишияма, С .; Икеноути, Х .; Кикучи, А .; Изуми, Р .; и другие. Фокальный сегментарный гломерулосклероз, связанный с хронической прогрессирующей наружной офтальмоплегией и мутацией митохондриальной ДНК A3243G. Нефрон 2018, 138, 243–248. [Перекрестная ссылка]
111. Коннор, ТМ; Хёр, С.; Маллетт, А .; Гейл, ДП; Гомес-Дюран, А .; Поссе, В.; Антробус, Р .; Морено, П.; Шаковелли, М .; Фрезза, К.; и другие. Мутации в митохондриальной ДНК вызывают тубулоинтерстициальное заболевание почек. Генетика PLoS. 2017, 13, e1006620. [Перекрестная ссылка] [PubMed]
112. Адема, А.Я.; Янссен, MC; van der Heijden, JW Новая мутация в митохондриальной ДНК у пациента с диабетом, глухотой и протеинурией. Нет. Дж. Мед. 2016, 74, 455–457. [Пубмед]
113. Ng, Y.S.; Hardy, S.A.; Shrier, V.; Quaghebeur, G.; Mole, D.R.; Daniels, M.J.; Downes, S.M.; Freebody, J.; Fratter, C.; Hofer, M.; et al. Clinical features of the pathogenic m.5540G>Мутация гена триптофана в митохондриальной транспортной РНК. нервно-мышечная. Беспорядок. 2016, 26, 702–705. [Перекрестная ссылка] [PubMed]
114. Tabebi, M.; Mkaouar-Rebai, E.; Mnif, M.; Kallabi, F.; Ben, M.A.; Ben, S.W.; Charfi, N.; Keskes-Ammar, L.; Kamoun, H.; Abid, M.; et al. A novel mutation MT-COIII m.9267G>C and MT-COI m.5913G>Мутация в митохондриальных генах в тунисской семье с наследственным диабетом и глухотой по материнской линии (MIDD), связанная с тяжелой нефропатией. Биохим. Биофиз. Рез. коммун. 2015, 459, 353–360. [Перекрестная ссылка]
115. Имасава, Т.; Танака, М .; Ямагути, Ю.; Наказато, Т .; Китамура, Х .; Nishimura, M. 7501 T > Вариант митохондриальной ДНК у пациента с гломерулосклерозом. Рен Фэйл. 2014, 36, 1461–1465. [Перекрестная ссылка]
116. Сеидовский, А.; Хоффманн, М .; Гловацкий, Ф.; Даэненс, КМ; Дево, JP; де Сент, ФК; Провот, Ф.; Геербрант, JD; Хаммель, А .; Хаззан, М .; и другие. Поражение почек при синдроме MELAS — серия из 5 случаев и обзор литературы. клин. Нефрол. 2013, 80, 456–463. [Перекрестная ссылка]
117. Чан, В.; Ham, YH Исследование скрытой роли повреждения и дисфункции митохондриальной ДНК в этиологии аристолоховой кислотной нефропатии. хим. Рез. Токсикол. 2021, 34, 1903–1909. [Перекрестная ссылка]
118. Бринкманн, А.; Вайс, К.; Уилберт, Ф.; фон Мёрс, А.; Цвирнер, А .; Столтенбург-Дидингер, Г.; Вилиховский, Э.; Schuelke, M. Регионарная патология коррелирует с увеличением количества копий мтДНК у пациента с миоклонической эпилепсией с рваными красными волокнами (MERRF-синдром). PLoS ONE 2010, 5, e13513. [Перекрестная ссылка]
119. Якупчак, Дж. П.; Мара, С .; Марковиц, Мэн; Гринберг, А.К.; Хок, Миссури; Майтра, А .; Баркер, ЧП; Вагнер, ПД; Ром, ВН; Шривастава, С .; и другие. Эффективность мутаций митохондриальной ДНК для выявления рака на ранней стадии. BMC Cancer 2008, 8, 285. [CrossRef]
120. Юань Ю.; Ю, ЮС; Ким, Ю .; Ли, Дж.; Ван, Ю.; Юн, СиДжей; Ян, Ю .; Мартинкорена, И.; Крейтон, СиДжей; Вайнштейн, Дж. Н.; и другие. Комплексная молекулярная характеристика митохондриальных геномов при раке человека. Нац. Жене. 2020, 52, 342–352. [Перекрестная ссылка]
121. Маэкава, Х.; Иноуэ, Т .; Оучи, Х .; Джао, ТМ; Иноуэ, Р .; Ниши, Х .; Фуджи, Р .; Ишидате, Ф .; Танака, Т .; Танака, Ю.; и другие. Повреждение митохондрий вызывает воспаление посредством передачи сигналов cGAS-STING при остром повреждении почек. Cell Rep. 2019, 29, 1261–1273. [Перекрестная ссылка] [PubMed]
122. Фэн Ю.; Имам, АА; Томбо, Н.; Дрегер, Д.; Bopassa, JC Транслокация RIP3 в митохондрии способствует деградации митофилина, что увеличивает воспаление и повреждение почек после почечной ишемии-реперфузии. Cells-Basel 2022, 11, 1894. [CrossRef] [PubMed]
123. Чанг, К.В.; Диллон, П.; Хуанг, С .; Шэн, X .; Шреста, Р.; Цю, К .; Кауфман, Б.А.; Парк, Дж.; Пей, Л.; Баур, Дж.; и другие. Повреждение митохондрий и активация пути STING приводят к воспалению почек и фиброзу. Клеточный метаб. 2019, 30, 784–799. [Перекрестная ссылка] [PubMed]
124. Ито, С.; Накашима, М .; Исикирияма, Т .; Накашима, Х .; Ямагата, А .; Имакире, Т .; Киношита, М .; Секи, С .; Кумагаи, Х .; Ошима, Н. Влияние лечения L-карнитином на митохондрии почек и макрофаги у мышей с диабетической нефропатией. Почечный пресс крови Res. 2022, 47, 277–290. [Перекрестная ссылка]
125. Лю З.; Тиан, Дж .; Пэн, Ф .; Ван, Дж. Гиперметилирование митохондриальной ДНК способствует метастазированию почечно-клеточной карциномы в кости. Дж. Рак 2022, 13, 304–312. [Перекрестная ссылка]
126. Мякала, К.; Джонс, BA; Ван, ХХ; Леви, М. Лечение сакубитрилом/валсартаном имеет разные эффекты в модулировании диабетической болезни почек у мышей db/db и мышей KKAy по сравнению с лечением валсартаном. Являюсь. Дж. Физиол Рен. Физиол. 2021, 320, F1133–F1151. [Перекрестная ссылка]
127. Лю З.; Ли, Ю .; Ли, К .; Ю, Л.; Чанг, Ю.; Qu, M. Доставка коэнзима Q10 с помощью наноносителя, нацеленного на митохондрии, ослабляет почечное ишемически-реперфузионное повреждение у мышей. Матер. науч. англ. С Матер. биол. заявл. 2021, 131, 112536. [Перекрестная ссылка]
128. Дин М.; Толберт, Э.; Биркенбах, М.; Гох, Р .; Ахлаги, Ф .; Гонем, Н.С. Трепростинил снижает повреждение митохондрий при ишемии-реперфузии почек у крыс. Биомед. Фармацевт. 2021, 141, 111912. [Перекрестная ссылка]
129. Чжан, М.; Донг, Р .; Юань, Дж.; Да, Дж.; Жа, Ю .; Long, Y. Roxadustat (FG-4592) защищает от острого повреждения почек, вызванного ишемией/реперфузией, путем ингибирования пути повреждения митохондрий у мышей. клин. Эксп. фарм. Физиол. 2022, 49, 311–318. [Перекрестная ссылка]
130. Ю, Х.; Мэн, X .; Сюй, М .; Чжан, X .; Чжан, Ю .; Дин, Г .; Хуанг, С .; Чжан, А .; Jia, Z. Целастрол снижает нефротоксичность цисплатина путем ингибирования NF-kappaB и улучшения функции митохондрий. Эбиомедицина 2018, 36, 266–280. [Перекрестная ссылка]
131. Гонг, В.; Лу, Л.; Чжоу, Ю .; Лю, Дж.; Ма, Х .; Фу, Л.; Хуанг, С .; Чжан, Ю .; Чжан, А .; Jia, Z. Новый антагонист STING H151 улучшает вызванное цисплатином острое повреждение почек и митохондриальную дисфункцию. Являюсь. Дж. Физиол. Рен. Физиол. 2021, 320, F608–F616. [Перекрестная ссылка] [PubMed]
132. Чен Ю.; Ян, Ю .; Лю, З .; He, L. Адипонектин способствует восстановлению эпителиальных клеток почечных канальцев, регулируя биогенез и функцию митохондрий. Метаболизм 2022, 128, 154959. [CrossRef] [PubMed]
133. Сюэ, Х.; Ли, П.; Луо, Ю .; Ву, К .; Лю, Ю.; Цинь, X .; Хуанг, X .; Sun, C. Салидрозид стимулирует ось Sirt1/PGC-1альфа и облегчает диабетическую нефропатию у мышей. Фитомедицина 2019, 54, 240–247. [Перекрестная ссылка] [PubMed]
134. Хан П.; Кай, Ю .; Ван, Ю.; Венг, В .; Чен, Ю .; Ван, М .; Жан, Х .; Ю, Х.; Ван, Т .; Шао, М .; и другие. Артеметер улучшает повреждение почек, восстанавливая окислительно-восстановительный дисбаланс и улучшая функцию митохондрий при адриамициновой нефропатии у мышей. науч. Отчет 2021, 11, 1266. [CrossRef]
135. Зорова Л.Д.; Ковальчук, С.И.; Попков, В.А.; Черников, В.П.; Жарикова, А.А.; Хуторненко, А.А.; Зоров, С.Д.; Плохих, К.С.; Зиновкин, Р.А.; Евтушенко, Е.А.; и другие. Содержат ли внеклеточные везикулы, полученные из мезенхимальных стволовых клеток, функциональные митохондрии? Междунар. Дж. Мол. Sci 2022, 23, 7408. [Перекрестная ссылка]
136. Олсен, GM; Риндер, Х.М.; Торми, Калифорния Гемофилия, приобретенная впервые, как явление иммунной дисрегуляции после инфекции SARS-CoV-2. Переливание 2021, 61, 989–991. [Перекрестная ссылка]
137. Лю З.; Солнце, Ю.; Ци, З .; Цао, Л.; Дин, С. Митохондриальный перенос/трансплантация: новый терапевтический подход к множественным заболеваниям. Клетка Биоски. 2022, 12, 66. [Перекрестная ссылка]
138. Эрнандес-Крус, Э.Ю.; Амадор-Мартинес, И.; Аранда-Ривера, Аляска; Круз-Грегорио, А .; Pedraza, CJ Повреждение почек, вызванное кадмием, и его возможная терапия трансплантацией митохондрий. хим. биол. Взаимодействовать. 2022, 361, 109961. [Перекрестная ссылка]
139. Вентилятор, XY; Го, Л .; Чен, Л. Н.; Инь, С .; Вен, Дж.; Ли, С .; Ма, JY; Цзин, Т .; Цзян, MX; Солнце, XH; и другие. Снижение гетероплазмии мтДНК при митохондриальной заместительной терапии путем индукции форсированной митофагии. Нац. Биомед. англ. 2022, 6, 339–350. [Перекрестная ссылка]
Цзюнь Фэн 1,2, Чжаовэй Чен 1,2, Вэй Лян 1,2, Чжунпин Вэй 1,2 и Гохуа Дин 1,2,
1 Отделение нефрологии, Больница Жэньминь Уханьского университета, Ухань 430060, Китай
2 Научно-исследовательский институт нефрологии и урологии Уханьского университета, Ухань 430060, Китай






