Защитный эффект ресвератрола при почечной недостаточности, вызванной акриламидом
Feb 23, 2022
Фон: Акриламид (ACR) имеет широкий спектр применения. Он обладаетпочечная недостаточностьэффект. Работа была направлена на изучение возможной защитной роли ресвератрола (RVS) в отношении ACR-опосредованногопочечная недостаточностьу крыс. Были исследованы предполагаемые основные механизмы, участвующие в такой защите.Материалы и методы:Тридцать взрослых белых крыс Sprague-Dawley были разделены на три группы: контроль, ACR и RVS. Через 4 недели,почкабыл удален и подготовлен для гистологического, иммуногистохимического и биохимического исследования. Оценивали активность тканевых окислительных (малоновый диальдегид [МДА]) и антиоксидантных (глутатион [GSH]) маркеров.Полученные результаты:Клубочковая индуцированная акриламидомпочечныйпоражение в виде сморщивания и деформации клубочков со сморщиванием их базальных оболочек и расширением мочевыводящих путей. В проксимальных извитых канальцах выражены дегенеративные изменения канальцев. Некротические тубулярные клетки демонстрировали цитоплазматическую вакуолизацию с слущенными эпителиальными клетками в просвете канальцев. ACR увеличивает отложение коллагеновых волокон в базальной мембране капилляров клубочков и вызывает утолщение базальных мембран клубочков.почечныйтельца ипочечныйканальцы. Администрация RVS обеспечивает высокую степень защитыпочка. Клубочки ипочечныйканальцы почти в норме. Содержание коллагеновых волокон и периодокислотная реакция Шиффа базальной мембраныпочечныйканальцы были на 70 процентов и на 19 процентов ниже связаны с группой ACR. Уровни креатинина и мочевины снизились на 51 процент и 47 процентов. RVS индуцировал такую защитную роль благодаря своему антиоксидантному действию, поскольку уровень MDA снизился на 45 процентов, а уровень GSH увеличился на 83 процента по сравнению с группой ACR. Выводы. Акриламид вызывает структурно-функциональные нарушенияпочка.Это вызываетпочкаповреждения в результате окислительного стресса и апоптоза. При использовании РВС нормальнаяпочкаархитектура сохранилась с небольшими структурными изменениями. Добавление, функционалпочкатест стал нормальным. RVS оказывает защитное действие благодаря своим антиапоптотическим и антиоксидантным свойствам. (Фолиа Морфол 2021; 80, 4: 985–993).

ВВЕДЕНИЕАкриламид (ACR) является хорошо известным загрязнителем окружающей среды, который оказывает ряд системных токсических эффектов на людей как при профессиональном, так и при пищевом воздействии [2, 22]. Он обладает целым рядом вредных свойств: канцерогенностью, генотоксичностью, нейротоксичностью и репродуктивной токсичностью [5, 7]. ACR и его аналоги широко используются в различных химических и экологических приложениях и производятся путем нагревания биологического материала, полученного из тканей растений [25]. Образование АКР происходит при переработке пищевых продуктов за счет воздействия на углеводы температур выше 200°С [12]. Высокие уровни ACR были обнаружены, в частности, в широко потребляемых пищевых продуктах; картофельные чипсы и хлеб [31].
Акриламид всасывается из желудочно-кишечного тракта, широко распределяется в жидкостях организма и накапливается в печени ипочка[28]. Известно, что ACR вызывает структурные и функциональные изменения во многих органах.почечныйтубулярные клетки подвергаются дегенеративным вакуолярным изменениям, воспалительной клеточной инфильтрации и перигломерулярному отеку [28]. Кроме того, введение ACR крысам повышает уровни мочевины, креатинина, мочевой кислоты ипочечныйпровоспалительный цитокин [1]. Метаболизм ACR запускает высвобождение свободных радикалов (АФК), что инициирует окислительный стресс, приводящий к дисбалансу в развитии и деградации АФК [19]. Он также вызывает перекисное окисление липидов и повреждение ДНК [1].
Эффекты многих антиоксидантов и противовоспалительных соединений, таких как оливковое масло, витамин Е и 5-аминосалициловая кислота, были изучены для предотвращения и лечения ACR-индуцированногопочечная недостаточность[9, 19]. Ресвератрол (RVS) представляет собой фитоалексин, обнаруженный, по крайней мере, в72 вида растений, многие из которых употребляются в пищу человеком, включая шелковицу, арахис и виноград [8]. РВС обладает противовоспалительной, антиагрегантной, антиоксидантной и антиканцерогенной активностью, а также способностью снижатьповреждение почеквызванные химическими соединениями [8, 10]. Однако неясно, может ли RVS защищать от ACR-индуцированногопочечная недостаточностьили нет. Поэтому мы изучили окислительный и апоптотический повреждающий эффект ACR в течениепочкаи исследовал защитную роль РВС над такимипочечная недостаточностьу крыс.
Ключевые слова:ресвератрол, акриламид, почки, почечная, почечная недостаточность
МАТЕРИАЛЫ И МЕТОДЫ
ЖивотныеВ нашем исследовании приняли участие 30 взрослых крыс-альбиносов Sprague-Dawley весом 170–200 г. Животные содержались в просторных сетчатых клетках в специальном помещении с прямым дневным освещением и естественной вентиляцией. Крысы имели свободный доступ к стандартному крысиному корму и воде. Всех животных лечили в соответствии со стандартными рекомендациями по уходу и использованию лабораторных животных. Исследование было разрешено Комитетом по этике медицинского факультета Каирского университета, Египет.Применяемые процедуры соответствовали этическим стандартам ответственной организации и Хельсинкской декларации 1975 года, пересмотренной в 1983 году.
Экспериментальная дизайнКрысы были разделены на три группы (по 10 в каждой): контрольная (давали дистиллированную воду в дозе 1 мл), группа АКР и группа РВС (одновременно АКР плюс РВС).
ХимикатыАкриламид получали в контейнере с порошком, закупленным компанией Biostain (Великобритания) массой 500 г. Его растворяли в дистиллированной воде в концентрации 10 г/л. Его вводили в дозе 1 мл дистиллированной воды, содержащей 40 мг/кг/сутки, перорально через желудочный зонд [9]. Ресвератрол (чистота > 99 процентов) был приобретен у Sigma-Aldrich (Сент-Луис, Миссури, США). Его растворяли в диметилсульфоксиде и разбавляли 0,9% физиологическим раствором. Его назначали в суточной дозе 20 мг/кг/сут перорально через желудочный зонд [18]. К концу эксперимента (через 4 недели) каждое животное взвешивали и брали пробу крови из хвостовой вены с помощью тонкой гепаринизированной капиллярной трубки.почкаэкстрагировали, промывали физиологическим раствором и сушили на бумаге.
Световое микроскопическое исследованиеПочкаобразцы фиксировали в 10-процентном формалине, обезвоживали в этиловом спирте, просветляли в ксилоле и заливали в парафин. Были вырезаны срезы толщиной 5 мкм и помещены на предметные стекла. Другие срезы помещали на положительно заряженные предметные стекла для иммуногистохимии. Срезы подвергали следующим действиям: - срезы, окрашенные гематоксилином и эозином (H&E), и трихромом по Массону готовили в соответствии с Suvarna et al. [24]; - гистохимическая оценка: окраска периодической кислотой по Шиффу (PAS): срезы, окрашенные PAS, готовили в соответствии с Suvarna et al. [24]; иммуногистохимический анализ Bcl-2-ассоциированного Х-белка (ВАХ) [20]. Готовили парафиновые срезы. Затем к срезам добавляли подходящее количество сыворотки на 30 мин. Эндогенную пероксидазу инактивировали метанольным раствором, содержащим H2O2 (1:50), в течение 10 мин и промывали фосфатно-солевым буфером (PBS). Срезы ткани блокировали 1,5% сывороткой на 30 мин. Срезы инкубировали с первичным антителом Bax (анти-человеческий белок BAX, DakoCytomation, Дания), а затем с вторичным антителом (универсальное биотинилированное звено из коммерческого набора LSAB: DakoCytomation, Дания). Затем образцы инкубировали с ферментами АВ в течение 30 мин и промывали в PBS. Положительные сигналы детектировали с использованием хромогенных субстратов пероксидазы. Отрицательный контроль включал PBS вместо вторичного антитела.

Анализ изображений и морфометрические измеренияС помощью компьютерной системы анализатора изображений Leica LAS V3.8 (Швейцария) оценивались следующие параметры: диаметрыпочечныйклубочков и проксимальных извитых канальцев, ширинапочечныйпространства и высоты выстилки эпителия проксимальных канальцев. При добавлении количество структурно измененных клубочков оценивали в процентах от общего числа клубочков. Также оценивали содержание коллагеновых волокон. В окрашенных PAS гистологических срезах дополнительно определяли оптическую плотность базальной мембраны проксимальных извитых канальцев и пристеночных слоев боуменовых капсул. В области иммуногистохимического окрашивания BCL2 также измеряли процент иммунной реакции.
Биохимическое исследованиеОбразцы крови, взятые у крыс перед умерщвлением, использовали для биохимической оценки в отделе биохимии и молекулярной биологии медицинского факультета Каирского университета, Египет.
Уровни мочевины и креатинина в сывороткеоценивали обычным колориметрическим методом с использованием наборов Quanti Chrom TM Assay Kits (DIUR-500 и DICT-500) на основе усовершенствованных методов Юнга и Яффе соответственно [32]. Средние значения этих биохимических показателей рассчитывали и подвергали статистическому анализу.
Тканевой уровень малонового диальдегида (МДА) и восстановленного глутатиона (GSH).почечныйткань гомогенизировали в 5–10 мл холодного буфера (50 мМ фосфата калия, рН 7,5, 1 мМ ЭДТА) на грамм ткани, затем центрифугировали при 100,000 g в течение 15 мин при 4°С. Супернатант удаляли для анализа и хранили на льду. Анализ малонового диальдегида проводили с тестом на тиобарбитуровую кислоту (ТБК) в супернатанте по методу, предложенному Buege и Aust [4].МДА реагирует с ТБА с образованием соединения красного цвета, поглощающего при 535 нм. Измерение GSH было основано на восстановлении 5,5-дитиобис(2-нитробензойной кислоты) (DTNB) восстановленным GSH с образованием соединения желтого цвета [6].
статистический анализСредние значения относительныхпочкавес, гистоморфометрические измерения и биохимические уровни были проанализированы с использованием SPSS версии 22. Статистическая оценка была выполнена с использованием ANOVA с последующим попарным сравнением Бонферрони.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ
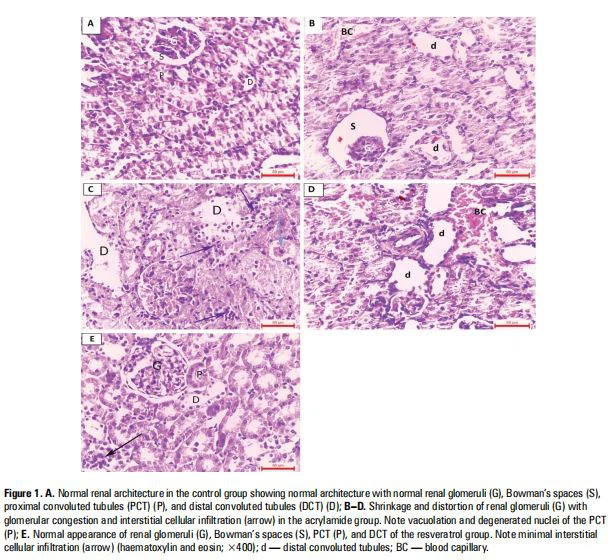
Световая микроскопияОбследование контрольной группы показало интактную архитектурупочечныйкора.почечныйкора образованапочечныйтельца, а также проксимальные и дистальные извитые канальцы (рис. 1А). Экспертизапочечныйв коре группы ACR обнаружены выраженные структурные изменения.почечныйклубочки показали умеренную или выраженную усадку, деформацию, сегментацию и вакуолизацию с расширением мочевых пространств.почечныйканальцы были расширены с выраженным уменьшением их эпителиальной высоты и расширением их просвета. Клетки их выстилки демонстрировали цитоплазматическую вакуолизацию, клеточную фрагментацию и формирование внутрипросветных цилиндров во многих извитых канальцах. В интерстиции были обнаружены перегруженные кровеносные сосуды с утолщением интимы, а также можно было увидеть массивную клеточную инфильтрацию (рис. 1B-D). Обследование группы РВС выявило почти нормальный вид большинства клубочков и канальцев. Встречалась минимальная интерстициальная воспалительная клеточная инфильтрация (рис. 1Е).
Содержание коллагеновых волоконСодержание клетчатки было минимальным в контрольной группе. Содержимое увеличивалось вокруг пристеночных слоев боуменовой капсулы и базальных мембранпочечныйканальцы в группах ACR (9-fold) и RVS (2-fold) по отношению к контрольной группе. Содержание в группе RVS было на 70 процентов ниже, чем в группе ACR (рис. 2A–C, таблица 1).
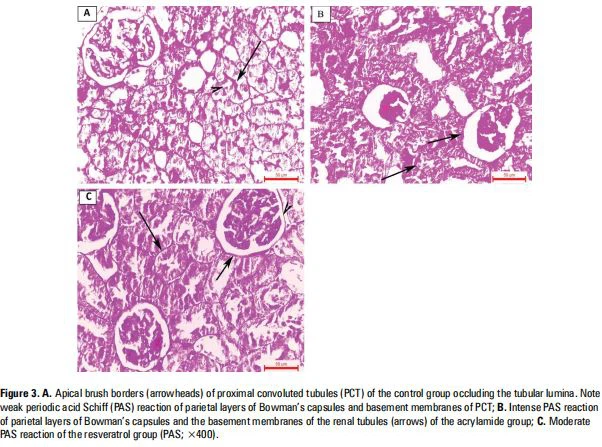
Гистохимия почкиВ контрольной группе базальные мембраныпочечныйканальцах и пристеночных листках боуменовой капсулы характеризовалась слабой PAS-реакцией. Добавляя, апикальные щеточные края проксимальной извитой
канальцы (PCT) были интактными и частично закрывали просвет канальцев (рис. 3А). Базальные мембраныпочечныйканальцы и пристеночные листки боуменовой капсулы группы ACR показали интенсивную PAS-реакцию (на 42% выше, чем в контрольной группе). При добавлении апикальные щеточные границы ПКТ были ослаблены (рис. 3В). При использовании РВС реакция PAS стала сравнима с контрольной группой и была на 19% ниже, чем в группе ACR (рис. 3В, табл. 1).
Иммуногистохимическое окрашивание BAXBAX показал слабую реакцию в контрольной группе (рис. 4А). Процент площади BAX-иммунопозитивных клеток увеличился в 4,5- раза в группе ACR, соответствующей контрольной группе (рис. 4B, C, таблица 1). При использовании RVS процент площади иммунопозитивных клеток уменьшился на 56 процентов, что соответствует группе ACR; однако процент площади в группе RVS был в 1,4- раз выше, чем в контрольной группе (рис. 4D, таблица 1).
Биохимические и окислительные/антиоксидантные маркерыУровни креатинина и мочевины в сыворотке увеличились в группе ACR в 2,75- раза, в 1,9-раз по сравнению с контрольной группой. При одновременном применении РВС уровни креатинина и мочевины снизились на 51%, что на 47% связано с АКР. Тем не менее, уровни креатинина и мочевины в группе RVS были на 83 процента, что на 55 процентов выше, чем в контрольной группе (таблица 1).


Значения окислительного маркера (MDA) в группе ACR увеличились в 1,4-раз, а антиоксидантного маркера (GSH) снизились в 1,3-раза по сравнению с контрольной группой. При использовании РВС уровень МДА снизился на 45 процентов, а уровень GSH увеличился на 83 процента по сравнению с группой АКР. Тем не менее, уровень обоих маркеров был ниже контрольной группы (таблица 1).
Морфометрические клубочковые и ПКТ измененияПроцент пораженных клубочков в группе ACR увеличился в 8,8- раз по сравнению с контрольной группой. При использовании РВС процент пораженных клубочков уменьшился на 71 процент, что соответствуетгруппа АКР; однако процент в группе RVS был в 1,6-раз выше, чем в контрольной группе (таблица 2).

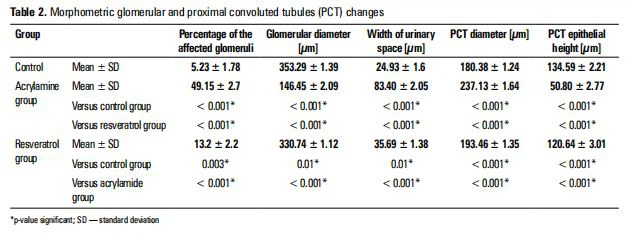
В группе ACR диаметр клубочков уменьшился на 58% при увеличении ширины мочевого пространства в 2,4- раза по сравнению с контрольной группой. При использовании РВС диаметр клубочков увеличился в 1,26- раз с уменьшением ширины мочевого пространства на 57 процентов, что соответствует группе ACR. Диаметр клубочков и ширина мочевого пространства в RVS и контрольной группе были одинаковыми (табл. 2). В группе ACR диаметр ПКТ увеличился на 31 процент, а высота эпидермиса их подкладки увеличилась.телий снизился на 62 процента по сравнению с контрольной группой. При использовании РВС диаметр ПКТ уменьшился на 18 процентов, а высота эпителия их выстилки увеличилась в 1,4-раз, что соответствует группе ACR. Оба параметра были сопоставимы в РВС и контрольной группе (табл. 2).
ОБСУЖДЕНИЕКлубочковая индуцированная акриламидомпочечныйпоражение в виде сморщивания и деформации клубочков со сморщиванием их базальных оболочек и расширением мочевыводящих путей. Кроме того, дегенеративные тубулярные изменения заметно присутствовали в ПКТ. Некротические тубулярные клетки демонстрировали цитоплазматическую вакуолизацию с слущенными эпителиальными клетками в просвете канальцев. Кроме того, ACR индуцировала массивную воспалительную клеточную инфильтрацию с гиперемией гломерулярных кровеносных сосудов. Акриламид индуцировал фиброз, который был установлен по 9-кратному увеличению отложения коллагеновых волокон в базальной мембране гломерулярных капилляров. Такие коллагеновые волокна могут быть результатом действия эпидермального фактора роста, стимулирующего пролиферацию фибробластов и синтез коллагена [14].Базальные мембраныпочечныйтельца ипочечныйканальцы группы ACR показали интенсивную PAS-реакцию (на 42% выше, чем в контрольной группе). Утолщение базальной мембраны канальцев является общим признаком атрофии и может быть связано с гиалинозом [14]. Утолщение также является возможной причиной снижения активного транспорта при ПКТ, вызывая микроальбуминурию [14].
Щеточная граница ПКТ в группе ACR была прервана. Потеря щеточной каймы является наиболее ранним морфологическим признаком нарушения функции проксимальных канальцев [17, 27]. Кроме того, потеря щеточной каймы влияет на реабсорбционную способность ПКТ с потерей глюкозы, солей и большого количества воды с мочой [17, 27]. Этим в основном объясняются наблюдаемые серологические изменения (повышение уровня мочевины и креатинина в сыворотке крови). Диаметр ПКТ увеличился на 31 процент в группе ACR, что в основном является компенсаторным механизмом для сохраненияфункция почек [15].
Окислительный стресс является основным патогенетическим механизмом, посредством которого ACR индуцируетпоражение почек. Окислительный стресс представляет собой сдвиг баланса между оксидантами и антиоксидантами в пользу оксидантов [3]. Многие исследователи доказали роль ACR в окислительном стрессе в течениепочка[23]. Значения окислительного маркера (MDA) в группе ACR увеличились в 1,4-раз, а антиоксидантного маркера (GSH) снизились в 1,3-раз. Окислительный стресс создает свободные радикалы кислорода (АФК), которые реагируют с многочисленными биомолекулами в клетке, что в конечном итоге приводит к окислительному повреждению [16]. АФК удаляются несколькими клеточными защитными механизмами с участием неферментативных (GSH). Белки пероксидазы GSH превращают перекись водорода в воду и липид.пероксидов в соответствующие им спирты [30]. Длительное применение ACR снижало активность GSH. Это следствие увеличения производства O2- и H2O2, что приводит к производству OH- [11]. Многие исследователи считали, что уровень МДА является достаточным доказательством окислительного стресса [13], а более высокое значение МДА свидетельствует об увеличении перекисного окисления липидов.

Апоптоз также является еще одним патогенетическим механизмом, посредством которого ACR индуцируетпочечныйпривязанность [23]. Реакция BAX увеличилась в 4,5- раза в группе ACR. BAX проявляет проапоптотическую активность [29]. Ресвератол, как один из флавоноидов, обеспечивает высокую защитупочкакак клубочки ипочечныйканальцы почти в норме. По сравнению с группой ACR содержание коллагеновых волокон и PAS-реакцияпочечныйканальцы уменьшились на 70,19 процентов. При добавлении уровень креатинина и мочевины снизился на 51,47 процента. Многие исследователи фиксируют экзогенный антиоксидантный защитный эффект РВС в течениепочка[21]. RVS индуцировал такую защитную роль благодаря своему антиоксидантному действию, поскольку уровень MDA снизился на 45 процентов, а уровень GSH увеличился на 83 процента по сравнению с группой ACR. RVS предотвращает продукцию супероксида несвязанной эндотелиальной синтазой оксида азота и увеличивает экспрессию различных антиоксидантных ферментов [30]. Антиоксидантная активность многих флавоноидов обусловлена прямым удалением свободных радикалов кислорода или возбужденных форм кислорода, а также ингибированием окислительных ферментов, продуцирующих АФК [26]. Другой защитный механизм против РВС заключается в его антиапоптотическом эффекте. При использовании RVS процент площади иммунопозитивных клеток BAX уменьшился на 56 процентов по сравнению с группой ACR.
ВЫВОДЫТаким образом, ACR вызывает структурные и функциональные нарушенияпочка. Это вызываетповреждение почекчерез окислительный стресс и апоптоз. При использовании РВС нормальнаяпочкаархитектура сохранилась с небольшими структурными изменениями. RVS обеспечивает защиту благодаря своим антиапоптотическим и антиоксидантным свойствам.
