Защитный эффект Cistanche Deserticola при повреждении печени: алкогольное поражение печени
Mar 19, 2022
Абстрактный:Современные фармакологические исследования показали, чтоЦистанхеDeserticola (C. Deserticola) оказывает защитное действие на печень, но его активная фракция и механизм не ясны. Чтобы определить эффективную фракцию C. Deserticola YC Ma, модель острого алкогольного повреждения печени у мышей была создана с 56-доказательством Erguotou и различными фракционными экстрактами C. Deserticola YC Ma (общие гликозиды, полисахариды и олигосахариды). ) вводили. После 14 дней перорального приема измеряли патологию печени и отложение липидов, а также экспрессию ядерного фактора Е2-родственного фактора (Nrf-2), kelch-подобного белка, ассоциированного с ЕСГ-1 ( Keap-1) и белок, ассоциированный с пузырьками плазмалеммы-1 (PV1), измеряли с помощью иммунофлуоресценции. Уровни аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), эндотоксина (ЭТ), диаминоксидазы (ДАО) и D-молочной кислоты (D-LA) в сыворотке, а также супероксиддисмутазы (СОД), глутатионпероксидазы (GSH -Px), каталазу (CAT) и малоновый диальдегид (MDA) в печени измеряли с помощью ELISA. Все эксперименты на животных проводились с одобрения Комитета по этике благополучия экспериментальных животных Центра медицинских наук Пекинского университета. Результаты показывают, что общее количество гликозидов C. Deserticola YC Ma (400 мг·кг-1) может уменьшать патологию печени, снижать сывороточный эндотоксин, диаминоксидазу и D-молочную кислоту, а также уменьшать отложение липидов в печени. Суммарные гликозиды также способствовали переносу Nrf-2 в ядро и снижали экспрессию Keap-1 и PV1. Таким образом, суммарные гликозиды C. Deserticola YC Ma оказывали защитное действие при остром алкогольном поражении печени, и этот механизм может быть связан с активацией пути Nrf-2/Keap-1, улучшением кишечной целостность стенок и торможение транспорта вредных веществ в печень.
Ключевые слова:Цистанхепустынная YC Ма; алкогольная болезнь печени; общие гликозиды C. Deserticola YCMa; защита печени; Путь Nrf-2/Keap-1
Защитный последствия из в общий гликозиды из Цистанхе пустыня Y. C. Ма в алкоголик печень рана в мышей
Контактное лицо: ali.ma@wecistanche.com

Алкогольная болезнь печени (АЛП) относится к заболеванию печени, вызванному длительным пьянством, которое обычно проявляется в виде алкогольной жировой дистрофии печени на начальной стадии, а затем перерастает в алкогольный гепатит, фиброз печени, цирроз печени и даже печеночную недостаточность [1]. ]. В последние годы с улучшением жизненного уровня населения увеличивается доля больных алкогольной болезнью печени, представляющей серьезную опасность для здоровья людей [2]. Исследования показали, что ALD в основном является результатом взаимодействия множества факторов, таких как воспалительная реакция, окислительный стресс и кишечные эндотоксины, прямо или косвенно индуцированные этанолом и его метаболитами, особенно эндотоксины кишечного происхождения, вызванные нарушением работы кишечника. барьерная функция. Эндотоксемия и эндотоксиновая активация клеток Купфера играют важную роль в возникновении и развитии АБП [3].
Традиционная китайская медицинаЦистанхеэто сочный стебельЦистанхеDeserticola (C. Deserticola) YC Ma илиЦистанхетрубчатый(Schenk) R. Wight растения Lidanaceae с сухими чешуйчатыми листьями. Исследования показали, что Цистанхе может усиливать иммунную функцию организма, омолаживать, противодействовать радиации, окислению и перекисному окислению липидов, а также защищать от алкогольного повреждения печени [4-7]. Предыдущие исследования в основном были сосредоточены на цистанхе пустынной, и гепатопротекторный эффект цистанхе пустынной и ее активных компонентов не ясен. В этой статье на основе модели острого алкогольного поражения печени обсуждались гепатопротекторный эффект и механизм действия экстрактов из различных частей цистанхе пустынной, а также была предоставлена теоретическая основа для последующих исследований и разработок цистанхе пустынной в защите печени.

Материалы и методы
Лабораторные животные Здоровые мыши Куньмин, самцы, массой (22 ± 5) г, были приобретены у компании Beijing Weitong Lihua Laboratory Animal Technology Co., Ltd., номер лицензии SCXK (Пекин) 2016-0011, и выращены в Экспериментальный центр медицинского факультета Пекинского университета, комнатная температура 20 ~ 25 градусов, влажность 56 ~ 60 процентов. Все операции на экспериментальных животных проводились в строгом соответствии со стандартами Комитета по этике животных Школы медицины Пекинского университета (LA2019123).
Для подготовки и определения содержанияЦистанхеэкстракт пустырника. Метод приготовления и метод определения содержанияЦистанхеэкстракт Deserticola, о котором ранее сообщала исследовательская группа, упоминался как [8-10]. 10 кг цистанхе пустынного экстрагировали водой и этанолом, чтобы получить 3,7% полисахаридов, и элюат в очищенной воде концентрировали, чтобы получить 38% густую пасту от общего количества олигосахаридов, элюировали 40% этанолом и сушили, чтобы получить 3,7% от общего количества гликозидов. . Эти 3 экстракта были использованы для экспериментальных исследований соответственно.
(G1260), набор для определения активности аланинаминотрансферазы (ALT) (номер партии BC1555) и набор для определения активности аспартатаминотрансферазы (AST) (номер партии BC1560) были приобретены у компании Beijing Soleibo Biotechnology Co., Ltd.; Набор супероксиддисмутазы (SOD) (партия A001-3), набор глутатионпероксидазы (GSH-Px) (партия A005), набор Malondialde (партия A005) - hyde, MDA) (партия A003-1), набор для обнаружения каталазы (каталазы, CAT) (A007-1), набор эндотоксина (ET) (E039- 1- 1), набор диаминоксидазы (DAO) (A088-2-1) и D-молочная кислота все наборы (D-LA) (H263) были получены от Nanjing Jiancheng Institute of Bioengineering; Бифениловый диэфир (бифендат, BIF, номер партии: S4890) был предоставлен Shanghai Lanmu Chemical Co., Ltd.; 56 процентов (содержание алкоголя 56 процентов) Hongxing Erguotou было предоставлено Beijing Hongxing Co., Ltd.; белок 1, ассоциированный с везикулами плазматической мембраны (плазма-лемма везикул), ассоциированный с белком -1, PV1) антитело (ab32570), антитело, родственное ядерному фактору E2 (Nrf-2), и kelch-подобный ECH-asso -циированный белок -1 (Keap) -1) (ab66620) приобретали у Abcam.
Экспериментальные инструменты Парафиновый микротом (Leica, Германия); микропланшет-ридер Sunrise-Basic (TECAN, Швейцария); высокоскоростная центрифуга с охлаждением (Beckman, США); инвертированный флуоресцентный микроскоп (IX73) (Olympus, Япония).
Подготовка и группировка мышиной модели острого алкогольного поражения печени. Шестьдесят здоровых самцов мышей Куньмин были взвешены, 1 0 в нормальной группе (NOR), а остальным мышам вводили Hongxing Erguotou через желудочный зонд [9]. в дозе 0,01 мл г - 1 через зонд, один раз в день в течение 7 дней подряд. Через 7 дней они были случайным образом разделены на модельную группу (MOD), бидентатную группу (BIF, 0,9 мг/кг-1) и группу общих гликозидов (ТГ, 400 мг/кг-1) в зависимости от массы тела. ),Цистанхегруппа полисахаридов пустыни (PS, 400 мг·кг-1) и группа олигосахаридов Cistanche Deserticola (ОС, 400 мг·кг-1), а дозировка была установлена в соответствии с предыдущим исследованием исследовательской группы[ 11]. Каждой группе давали физиологический раствор, бифениловый диэфир, общие глюкозидыЦистанхеDeserticola, полисахарид Cistanche Deserticola и олигосахарид Cistanche Deserticola соответственно через желудочный зонд в течение 14 дней. Все лекарства готовили на физиологическом растворе. Из-за постоянного введения алкоголя через желудочный зонд некоторые мыши погибли, и последнее введение Экспериментальные реагенты Окрашивающий раствор HE (G1120), Окрашивающий раствор Oil red O, 8 на группу.
Через 30 мин после последнего введения получали коэффициент каждого органа мышей, и каждый орган получали по следующей формуле: коэффициент органа=[влажный вес органа (г)/вес тела крысы (г )] × 100 процентов для расчета каждого органа. Статистический анализ проводили с использованием программного обеспечения SPSS 19.0.

Окрашивание HE После того, как вышеупомянутые ткани печени были зафиксированы фиксатором тканей, срезы обычным образом заливали в парафин, окрашивали гематоксилин-эозином (HE) и наблюдали гистопатологические изменения под световым микроскопом.
Для индексного определения брали сыворотку мышей каждой группы и определяли содержание АЛТ, АСТ, ЭТ, ДАО и Д-ЛК согласно инструкции к набору. Мышей умерщвляли для удаления печени и готовили гомогенат ткани печени. Согласно инструкции к набору, активность КАТ, СОД, GSH-Px и содержание МДА.
Окрашивание масляным красным O брали фиксированную ткань печени мыши и помещали ее в 30-процентный раствор сахарозы. После того как ткань печени оседала на дно, ее переносили в 20-процентный раствор сахарозы. , толщина среза 100 мкм. Добавьте по каплям 1 × PBS для промывания на 10 минут, затем поместите его в 60-процентный изопропанол для погружения на 20-30 с; затем добавьте его в раствор для окрашивания модифицированным масляным красным O и запечатайте на 10-15 мин; помещают на некоторое время в 60-процентный раствор изопропанола. Промывают для удаления раствора красителя, ополаскивают водопроводной водой в течение 10 мин, заключают в глицерин-желатин, наблюдают и фотографируют под микроскопом.
Парафиновые срезы депарафинизировали и регидратировали для иммунофлуоресцентного химического окрашивания, а антиген извлекали с помощью цитрата натрия. Первичные антитела PV1 (1:200), Nrf-2 (1:100) и Keap-1 (1:200) добавляли по каплям, и клетки инкубировали при 4 градусах в течение ночи. Промыть PBS, добавить по каплям флуоресцентное вторичное антитело TRITC (1:100) и инкубировать в течение 1 ч при комнатной температуре в темноте. Ядра окрашивали Hoechst 33258, заливали антифлуоресцентной средой для распада в темноте и фотографировали под флуоресцентным микроскопом.
Окрашенные TUNEL парафиновые срезы депарафинизировали и регидратировали, добавляли по каплям 20 мкг·мл-1 разведения протеиназы К без ДНКазы, реакцию проводили при 37°С в течение 30 мин, затем 3 добавляли по каплям процентный раствор H2O2 и инкубировали при комнатной температуре в течение 20 мин. Промыть три раза 0,01 моль·л - 1 буферного раствора PBS; добавить по каплям 50 мкл раствора для мечения биотином, инкубировать при 37°С в течение 60 мин для остановки реакции; добавляют по каплям 50 мкл рабочего раствора стрептавидин-ТРИТЦ, инкубируют при комнатной температуре в течение 30 мин в темноте, ядра окрашивают DAPI, наносят на предметные стекла, просматривают под микроскопом и фотографируют с помощью флуоресцентного микроскопа.
Статистический анализ проводили с использованием программного обеспечения SPSS 19.0. Данные измерений выражали как среднее ± стандартное отклонение (x-±s), а данные измерений с нормальным распределением сравнивали с помощью однофакторного дисперсионного анализа (ANOVA) между группами. Если дисперсия была однородной, применялся метод СНК, а если дисперсия была неравной, применялся метод Даннета. Метод T3, подсчет данных с использованием теста хи-квадрат (критерий хи-квадрат), использование GraphPad Prism 5 для картирования данных, уровень наименьшей значимой разницы был установлен на уровне P <>
Результат
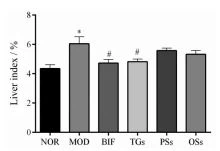
1 ТГ могут значительно снизить печеночный коэффициент у мышей с алкогольным поражением печени. Как показано на рисунке 1, по сравнению с группой NOR, печеночный коэффициент группы MOD значительно выше.
По сравнению с группой MOD печеночный коэффициент был значительно снижен после вмешательства ТГ, в то время как ФС и ОС не влияли на печеночный коэффициент, и не было существенной разницы между ТГ и BIF.
2 ТГ могут значительно улучшить патологическую морфологию ткани печени у мышей с алкогольным поражением печени.
Результаты окрашивания HE показали, что клетки ткани печени в группе NOR имели нормальную морфологию, аккуратно расположенные клетки, равномерное окрашивание, полную клеточную структуру и плотные межклеточные пространства; группа МОД имела неупорядоченное строение, неравномерное расположение клеток, рыхлые межклеточные пространства и нечеткие границы клеток; BIF и TGs После вмешательства изменение морфологии клеток было значительно лучше, чем у модельной группы, а количество клеток было больше, чем у модельной группы. Не было существенной разницы между ТГ и БИФ, а в группах ФС и ОС не было значительного улучшения патологической морфологии печени, что указывает на то, что ТГ обладают гепатопротекторным действием. Однако PS и OS не показали значительного улучшения, как показано на рисунке 2.

3 ТГ могут значительно уменьшить отложение липидов в печени у мышей с алкогольным поражением печени.
Окрашивание масляным красным O показало небольшое количество отложений липидов в группе NOR, в то время как отложение липидов в группе MOD было значительно увеличено; по сравнению с группой MOD отложение липидов было значительно уменьшено после вмешательства TGs; не было существенной разницы между ТГ и БИФ; ФС и ОС не влияли существенно на отложение липидов в печени. Экспериментальные результаты показали, что ТГ могут снижать отложение липидов в печени у мышей с алкогольным поражением печени, в то время как ФС и ОС не улучшают отложение липидов в печени у мышей с алкогольным поражением печени и не оказывают гиполипидемического эффекта (рис. 3).

4 ТГ могут значительно снизить уровни АЛТ и АСТ в печени у мышей с алкогольным поражением печени.
Результаты, представленные на рисунке 4, показывают, что по сравнению с группой НОР уровни АЛТ и АСТ в группе МОД были значительно повышены; по сравнению с группой МОД уровни АЛТ и АСТ в группе ТГ были значительно снижены; не было существенной разницы между ТГ и БИФ; Уровни АЛТ и АСТ существенно не изменились, что указывает на то, что ТГ ингибируют повреждение печени и обладают гепатопротекторным действием.
5 ТГ могут значительно ингибировать апоптоз клеток печени у мышей с алкогольным поражением печени.
После того, как алкоголь повреждает гепатоциты, ДНК в ядре разрушается, и окрашивание TUNEL показывает положительную экспрессию. Как показано на рисунке 5, большое количество клеток печени группы MOD подверглось апоптозу. По сравнению с группой MOD, апоптоз группы TGs был значительно снижен, и не было существенной разницы между TGs и BIF. Не было никаких существенных изменений, указывающих на то, что ТГ могут ингибировать апоптоз.
6 ТГ могут значительно улучшить патологическую морфологию тонкого кишечника у мышей с алкогольным поражением печени.
Результаты окрашивания HE показали, что гистологические клетки тонкой кишки в группе NOR имели нормальную морфологию, аккуратно расположенные ворсинки, однородную кишечную стенку, неповрежденную клеточную структуру и плотные межклеточные пространства; группа МОД имела неупорядоченное строение, неравномерное расположение ворсинок, трещиноватость и тонкую стенку кишечника; БИФ и ТГ После вмешательства значительно изменилась морфология клеток, утолщена кишечная стенка. В группах PS и OS не наблюдалось значительного улучшения патологической морфологии тонкой кишки, что указывает на то, что ТГ оказывали защитное действие на целостность кишечной стенки и ворсинок, как показано на рисунке 6.


7 ТГ значительно снижают экспрессию белка PV1 в стенке тонкого кишечника мышей с алкогольным поражением печени.
Белок PV1 представляет собой интегральный мембранный гликопротеин типа II, который является индикатором проницаемости кишечного сосудистого барьера, и его экспрессия была обнаружена с помощью иммунофлуоресцентного окрашивания для наблюдения за влиянием экстракта Cistanche Deserticola на проницаемость стенки кишечника. Как показано на рисунке 7, по сравнению с группой NOR уровень экспрессии белка PV1 в стенке тонкого кишечника группы MOD был значительно повышен; по сравнению с группой MOD уровень экспрессии белка PV1 в группе TGs был значительно снижен; ТГ имели значительные отличия по сравнению с BIF; в то время как PS. Не было значительных изменений в экспрессии белка PV1 между двумя группами и группой OS, что указывает на то, что TG могут способствовать восстановлению стенки тонкой кишки.

8 TG могут значительно улучшить содержание ET, DAO и D-LA в сыворотке у мышей с алкогольным поражением печени.
Результаты, показанные на рисунке 8, показывают, что по сравнению с группой NOR уровни ET, DAO и D-LA в сыворотке в группе MOD были значительно повышены; по сравнению с группой МОД уровни ЭТ, ДАО и Д-ЛК в группе ТГ были значительно снижены; Достоверных изменений в содержании этих показателей в группе не произошло.
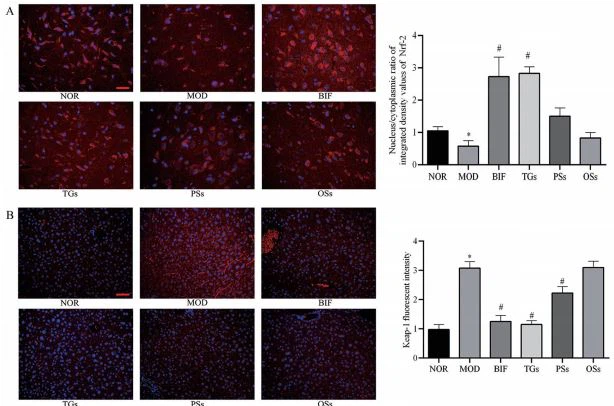
9 TG активируют сигнальный путь Nrf-2/Keap-1 в ткани печени мышей с алкогольным поражением печени.
Результаты иммунофлуоресцентного окрашивания показали, что по сравнению с группой NOR скорость проникновения в ядро Nrf-2 в печени группы MOD была значительно снижена; уровень экспрессии белка Keap-1 был значительно повышен; по сравнению с группой MOD, скорость проникновения в ядро Nrf-2 группы TGs была значительно увеличена; Уровень экспрессии белка Keap-1 был значительно снижен; TG не имели существенной разницы по сравнению с BIF; Группы PS и OS не оказывали значительного влияния на проникновение в ядро Nrf-2 и экспрессию Keap-1, как показано на рисунке 9.
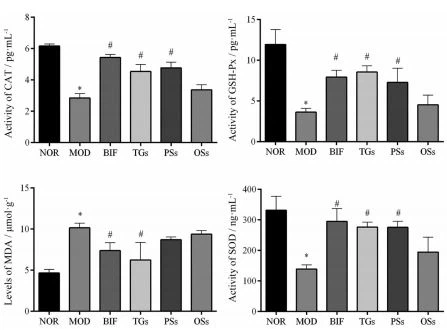
10 ТГ могут значительно улучшить уровни факторов окислительного стресса в ткани печени мышей с алкогольным поражением печени.
Данное экспериментальное исследование показало, что по сравнению с группой НОР активность СОД, КАТ и GSH-Px в группе МОД достоверно снижена, а содержание МДА значительно повышено; по сравнению с группой MOD активность SOD, CAT и GSH-Px была значительно увеличена после увеличения вмешательства BIF и TG, содержание MDA значительно снизилось, как показано на рисунке 10.

Обсуждение
В этом исследовании модель острого алкогольного поражения печени на мышах использовалась для изучения влияния экстрактов из различных частей цистанхе пустынной на острое алкогольное поражение печени при введении в течение 14 дней. , содержание АЛТ и АСТ в сыворотке крови и содержание МДА в ткани печени, достоверно повышали активность антиоксидантных ферментов СОД, КАТ и GSH-Px, улучшали морфологическую структуру ткани печени и проницаемость стенки кишечника, снижали в сыворотке ЭТ, ДАО и Д Содержание -LA ингибирует перенос бактериальных вторичных метаболитов в печень. В то же время суммарные глюкозиды цистанхе пустынной могут значительно способствовать проникновению Nrf-2 в ядро; ингибируют экспрессию белка Keap-1 и белка PV1 в стенке кишечника, что указывает на то, что общие глюкозиды Cistanche Deserticola могут активировать сигнальный путь Nrf-2/Keap-1 и восстанавливать стенку кишечника . повреждения для достижения защиты печени.
Цистанхе традиционной китайской медицины представляет собой сухой и чешуйчатый стебель цистанхе пустыни или цистанхе цистанхе, и общее количество гликозидов этих двух типов цистанхе в защите печени может улучшить морфологию ткани печени и уменьшить степень фиброза у крыс с фиброзом [12]. Исследовательская группа Luo Huiying [13] провела несколько исследований Cistanche Deserticola, и результаты показали, что общее количество глюкозидов Cistanche Deserticola может повышать активность SOD, GSH-Px и CAT в тканях печени мышей с алкогольным поражением печени. так же, как результаты этого исследования. Химические составляющие этих двух отличаются только содержанием фенилэтаноидных гликозидов, и наиболее изученным является Cistanche piensis. Исследования показали, что защитными для печени компонентами цистанхе пустынной являются, в основном, фенилэтаноидные гликозиды, но поскольку содержание фенилэтаноидных гликозидов в цистанхе пустынной ниже, чем в цистанхе пустынной, ее исследовали немногие. Если содержание ниже, чем у цистанхе Цистанхе, все же оказывает ли он гепатопротекторное действие. Сравнительное исследование других компонентов было проведено для уточнения компонентов, защищающих печень, а также для обеспечения экспериментальной основы действия цистанхе пустыни на защиту печени, а также для создания теоретической основы для последующей разработки продукта.

Развитие заболевания печени тесно связано с сигнальным путем Nrf-2/Keap-1, особенно с алкогольным поражением печени. Исследования показали, что этанол может индуцировать экспрессию белка 1, связывающего регуляторный элемент стерола (SREBP-1) у мышей Nrf-2-/-, а также может значительно повышать уровень триглицеридов в сыворотке [14]. Длительное употребление алкоголя может привести к активации Nrf-2 в печени мышей, тем самым снижая вызванный этанолом окислительный стресс. Окислительный стресс также тесно связан с возникновением и развитием заболеваний печени. Когда организм находится в состоянии окислительного стресса, Nrf-2 связывается с ядерными антиоксидантными ответными элементами (ARE) и затем инициирует экспрессию нижестоящих антиоксидантных генов. По сравнению с мышами дикого типа, мыши Nrf-2-/- более чувствительны к повреждению печени из-за их сниженной антиоксидантной способности и более восприимчивы к внешним раздражителям. Однако сверхэкспрессия белка Nrf-2 не показала явного повреждения печени [15]. Можно видеть, что активация Nrf-2 может быть новой потенциальной терапевтической мишенью и путем повреждения печени. В этом исследовании путем сравнения эффектов трех экстрактов цистанхе пустынной на острое алкогольное поражение печени было обнаружено, что общие глюкозиды цистанхе пустынной могут повышать активность антиоксидантных ферментов СОД, КАТ и GSH-Px путем активации Nrf{{ 19}}/Keap-1 сигнальный путь и, таким образом, играют роль в активации сигнального пути Nrf-2/Keap-1. Роль защиты печени.
Злоупотребление алкоголем является основным фактором, вызывающим алкогольное поражение печени, а алкоголь может способствовать избыточному росту грамотрицательных бактерий в кишечнике пациентов с хроническим поражением печени. Воротная вена достигает печени, тем самым усугубляя повреждение печени [16]. Исследования показали, что у пациентов с ALD и на животных моделях как алкоголь, так и его метаболит ацетальдегид могут повышать проницаемость кишечника и пропускать в кровь вредные вещества, такие как липополисахарид (LPS) и D-LA [17]. Это исследование показало, что суммарные глюкозиды цистанхе пустынного могут снижать проницаемость алкоголя в кишечном тракте, тем самым уменьшая содержание ЛПС, ДАО и Д-ЛК в крови и предотвращая попадание вредных веществ в печень через воротную вену. , тем самым играя роль в защите печени.
Бифендат — первое лекарство для лечения гепатита в моей стране. Он обладает фармакологическими эффектами, такими как снижение уровня ферментов, антиоксидантное и иммунное регулирование. Это исследование также показало, что бидентат оказывает значительное влияние на отложение липидов, и его действие может быть связано с его противовоспалительным действием. Окисление связано с улучшением состояния поврежденной ткани печени, тем самым улучшая метаболизм липидов в печени, но не сообщается, регулирует ли оно напрямую метаболизм липидов. В то же время из полученных результатов видно, что гепатопротекторное действие суммарных глюкозидов цистанхе пустынной существенно не отличается от такового бидентата, причем оба обладают антиоксидантным действием и снижают содержание ЭТ, ДАО и Д-ЛК в сыворотки, что означает, что общие глюкозиды Cistanche Deserticola не имеют существенной разницы. Существуют различия в одинаковой защите печени между гликозидами и бидентатом, что указывает на то, что бидентат не оказывает существенного влияния на снижение проницаемости кишечника, и его механизм снижения сывороточного ET, DAO и D-LA еще предстоит изучить.
Подводя итог, можно сказать, что общее количество глюкозидов цистанхе пустынного является активным участком препарата традиционной китайской медицины цистанхе пустынного, который может снижать окислительный стресс в печени и ингибировать поступление вредных кишечных веществ в печень, а также играть защитную роль при остром алкогольном опьянении. поражение печени. Его механизм может быть связан с активацией сигнального пути Nrf-2/Keap-1; в то время как полисахариды и олигосахариды Cistanche Deserticola не оказывают защитного действия на острое алкогольное поражение печени. Соответствующие результаты исследований дают полезную информацию для дальнейших исследований и разработок Cistanche Deserticola.

Для защиты печени с помощью cistanche para que sirve
использованная литература
[1] Чжан Ю.В., Ли Ю.Дж., Ху Б.Ф. и др. Оценка на трех краткосрочных животных моделях алкогольной болезни печени [J]. Acta Pharm Sin, 2018, 53: 236-243.
[2] Vonghia L, Leggio L, Ferrulli A, et al. Острая алкогольная интоксикация [J]. Eur J Intern Med, 2008, 19: 561-567.
[3] Хоу Дж., Лу Ю, Чжан Д.К. Связь между дисбактериозом кишечника и заболеваниями печени [J]. J Clin Hepatol, 2018, 34: 1128- 1132.
[4] Лю Ю, Ван Х, Ян М и др. Полисахариды Cistanche Deserticola защищают клетки PC12 от повреждений, вызванных OGD/RP [J]. Биомед Фармакотер, 2018, 99: 671-680.
[5] Сонг Д.З., Цао З., Лю З.Б. и др. Полисахарид цистанхе пустыни ослабляет остеокластогенез и резорбцию костей за счет ингибирования передачи сигналов RANKL и выработки активных форм кислорода [J]. J Cell Physiol, 2018, 233: 9674-9684.
[6] Чжан А.Л., Ян С.М., Ли QX и др. Иммуностимулирующая активность водоэкстрагируемых полисахаридов из Cistanche Deserticola в качестве растительного адъюванта in vitro и in vivo [J]. PLoS One, 2018, 13: e0191356.
[7] Чжан Х., Сян З., Дуань Х. и др. Противоопухолевое и противовоспалительное действие олигосахаридов из экстракта Cistanche Deserticola на повреждение спинного мозга [J]. Int J Biol Macromol, 2019, 124: 360-367.
[8] Ли Р.Ю., Чжао М.Б., Ту П.Ф. и др. Одновременное определение пяти фенилэтаноидных гликозидов в Cistanches Herba с использованием количественного анализа мультикомпонентов по одному маркеру [J]. J Chin Pharm Sci, 2019, 28: 537-546.
[9] Li SQ, Lu HJ, Wang P, et al. Изучение времени клеточного апоптоза при алкогольном поражении печени у мышей [J]. Chin J Clin Pharmacol, 2017, 33: 2154-2157.
[10] Ши З.И., Ву И., Чжу Ю.М. и др. Количественное определение бетаина, маннита, фруктозы, глюкозы и сахарозы в Cistanches 2019, 21: 1641- 1646.
[11] Гао Ю.Дж., Цзян И., Дай Ф. и др. Исследование слабительных компонентов Cistanche Deserticola YC Ma [J]. Mod Chin Med, 2015, 17: 307-310.
[12] You SP, Zhao J, Ma L, et al. Влияние и механизм действия гликозидов фенилэтаноидов Cistanche на крыс с иммунологическим фиброзом печени [J]. Chin J Pharmacol Toxicol, 2016, 30: 504-510.
[13] Luo HY, Liu Y, Xi GZ и др. Защитный эффект гликозидов Cistanchis на вызванное этанолом повреждение печени у мышей [J]. Chin J Clin Pharmacol Ther, 2009, 14:1225- 1228.
[14] Ву К.С., Лю Дж., Клаассен К.Д. Роль Nrf2 в предотвращении вызванного этанолом окислительного стресса и накопления липидов [J]. Toxicol Appl Pharmacol, 2012, 262: 321-329.
[15] Qu Q, Liu J, Zhou HH, et al. Nrf2 защищает от гепатотоксичности, вызванной фуросемидом [J]. Токсикология, 2014, 324: 35-42.
[16] Zhang L, Zu XP, Xie HS и др. Прогресс исследований механизма действия кишечных микроорганизмов при заболеваниях человека [J]. Acta Pharm Sin, 2016, 51: 843-852.
[17] Парлесак А., Шефер С., Шютц Т. и др. Повышенная проницаемость кишечника для макромолекул и эндотоксемия у больных хроническим алкоголизмом на разных стадиях алкогольного поражения печени [J]. Дж. Гепатол, 2000, 32: 742-747.
