Перекрестные помехи между микробиотой кишечника и иммунитетом хозяина: влияние на воспаление и иммунотерапию (2)
Oct 24, 2023
7.2. Желудочно-кишечные инфекции
В зависимости от контекста микробиота кишечника может либо защищать хозяина, либо увеличивать риск заражения экзогенными патогенами. Роль микробиома как защитной силы подтверждается исследованиями, показывающими, что незрелые микробиомы новорожденных более восприимчивы к инвазии патобионтов [222]. Существует несколько различных механизмов, с помощью которых комменсалы могут предотвращать колонизацию патогенами и защищать от инфекций, включая конкуренцию за ресурсы, высвобождение бактериофагов и продукцию антимикробных метаболитов [237–241]. Напротив, было показано, что метаболиты микробиома, такие как 4-метилбензойная кислота, 3,4-диметилбензойная кислота, гексановая кислота и гептановая кислота, увеличивают повреждение эпителия толстой кишки, как видно из энтерогеморрагической E. coli. в модели «орган-на-чипе» [223]. Более того, супернатант, взятый из комменсальной Escherichia albertii, также может повышать вирулентность диарейных видов E. coli, что приводит к TLR5-опосредованному увеличению IL-8 и общему усилению провоспалительной реакции кишечных клеток хозяина. [242]. Наличие определенных комменсалов и изменения в составе микробиома связаны с восприимчивостью к инфекциям таких организмов, как Clostridium difficile, Salmonella typhimurium, Escherichia coli, устойчивые к ванкомицину Enterococcus spp. и Citrobacter Rodentium [238, 239, 241, 243–245]. Одним из лучших примеров является CDI, где врожденные иммунные клетки стимулируются токсинами C. difficile через воспалительную сому и сигнальные пути TLR4, TLR5 и нуклеотид-связывающего домена олигомеризации белка 1 (NOD1) [246,247]. Многочисленные провоспалительные цитокины (такие как интерлейкин (IL)-12, IL-1, IL-18, гамма-интерферон (IFN-) и фактор некроза опухоли (TNF)) и хемокины (MIP-1a, MIP-2 и IL-8) впоследствии продуцируются, что приводит к увеличению проницаемости слизистой оболочки, дегрануляции тучных клеток, гибели эпителиальных клеток и нейтрофильной инфильтрации [248] . Важно отметить, что ИКД обычно является результатом вызванного антибиотиками нарушения микробиоты кишечника [249]. Уничтожение полезных бактерий в кишечнике с помощью некоторых антибиотиков, особенно клиндамицина, позволяет C. difficile процветать [250], что приводит к колиту и последующей диарее [251,252]. Помимо дисбактериоза кишечной микробиоты, популяции иммунных клеток, такие как клетки, экспрессирующие Th17- и IL-17-, могут способствовать рецидивированию CDI [253]. Для сравнения, ILC, активированные IL-33-, могут предотвратить CDI [254]. Поскольку истощение кишечной микробиоты является основной причиной ИКД, вмешательства, направленные на восстановление микробов, могут иметь терапевтическую ценность. Пребиотики, такие как пищевые волокна и их ферментированные побочные продукты, например, SCFA, являются возможными методами лечения ИКД. Например, пищевые волокна, такие как пектин, были способны восстанавливать эубиоз микробиоты кишечника (о чем свидетельствует увеличение количества Lachnospiraceae и уменьшение количества Enterobacteriaceae) и облегчение воспаления после колита, вызванного C. difficile [255]. Было также обнаружено, что бактерия, продуцирующая бутират, Clostridium Butyricum, защищает от CDI за счет увеличения количества нейтрофилов, клеток Th1 и Th17 на ранней фазе инфекции; это не зависело от передачи сигналов GPR43 и GPR109a [256]. Как упоминалось в разделе 6.2, CDI можно эффективно лечить с помощью FMT [152]. FMT также подтверждается в предыдущем исследовании, которое показало, что терапевтическое средство для микробной экосистемы, состоящее из 33 бактериальных штаммов, выделенных из стула человека, может лечить устойчивый к антибиотикам колит C. difficile [257]. Следует отметить, что аналогичные наблюдения наблюдались, когда терапия микробной экосистемы применялась при инфекции Salmonella typhimurium [258]. Эти результаты подчеркивают, что соответствующая модуляция микробиоты кишечника и иммунных реакций необходима для предотвращения инфекции и борьбы с ней.

последствия цистеина - лечите запор
7.3. Воспалительные заболевания кишечника
Воспалительные заболевания кишечника (ВЗК) развиваются из-за дефектов различных факторов, таких как окружающая среда, кишечные микробы, иммунная система и генетические факторы. ВЗК включает хроническое воспаление ЖКТ. Болезнь Крона (БК) и язвенный колит (ЯК) представляют собой два различных клинических состояния ВЗК, основанных на гистопатологических особенностях, локализации заболевания в ЖКТ и симптомах [259]. При ВЗК муколитические бактерии и патогенные бактерии разрушают слизистый барьер и усиливают инвазию патогенов в глубокие ткани кишечника [224, 260–262]. Изменения в составе микробиоты кишечника тесно связаны с развитием и прогрессированием ВЗК. У пациентов с ВЗК наблюдается снижение популяций Firmicutes и увеличение количества Proteobacteria, Bacteroidetes, Enterobacteriaceae и Bilophila [263–265]. Кроме того, многие виды провоспалительных бактерий покрыты IgA, как это наблюдается у пациентов с воспалительными заболеваниями кишечника и на мышиных моделях колита [266,267]. Кишечные микробы, по-видимому, играют прямую роль в развитии ВЗК на основании данных о том, что стерильные мыши защищены от колита [268]. Это подтверждается открытием, что имплантация кишечных микробов от мышей с ВЗК стерильным мышам привела к развитию ВЗК у последней группы [268]. Аналогичным образом, самки с ВЗК могут по существу передавать «микробиоту ВЗК» потомству, в результате чего у детенышей снижается микробное разнообразие и меньше В-клеток памяти с переключенным классом и Treg-клеток в толстой кишке [269]. Тесная связь между микробиотой и ВЗК продвинула вперед метагеномные подходы, помогающие лучше определять диагностические и терапевтические цели [270]. FMT предлагается в качестве потенциального метода лечения, при котором у пролеченных пациентов с ЯК было обнаружено повышенное содержание Faecalibaterium, что соответствовало меньшему количеству клеток ROR t + Th17 и большему количеству клеток Foxp3+ CD4+ Treg [166]. Также считается, что введение SCFAs является потенциальным терапевтическим средством для пациентов с воспалительными заболеваниями кишечника [271]. Подтверждающие данные включают опосредованное бутиратом ингибирование провоспалительных реакций нейтрофилов, т.е. НЭО, у мышей с колитом [272]. Существуют противоречивые сообщения о том, может ли пищевая клетчатка, предшественник SCFAs, быть полезным вмешательством для пациентов с воспалительным заболеванием кишечника. С одной стороны, было обнаружено, что специфическая смесь из нескольких волокон противодействует воспалению кишечника за счет увеличения количества клеток IL-10 и Treg [273]. Напротив, результаты наших исследований указывают на дихотомию в реакциях на пребиотические волокна у мышей с колитом, где пектин может облегчить воспаление по сравнению с инулином, что усугубляет патологию заболевания [274]. Более того, наше исследование показало, что бутират может быть вредным микробным метаболитом, усиливая воспалительную передачу сигналов NLRP3 [274]. Пробиотический коктейль, напротив, облегчал воспаление, переводя микробиоту кишечника на противовоспалительный профиль, который включал Akkermansia и Bifidobacterium [275]. В совокупности эти результаты указывают на то, что необходимы дополнительные исследования для понимания пребиотических волокон и SCFAs при воспалительных заболеваниях кишечника, прежде чем применять их в клиниках. Помимо SCFA, в воспалительном заболевании кишечника участвуют вторичные желчные кислоты. Хорошо известно, что DCA вызывает воспаление кишечника [276,277]. Частично это может быть связано с опосредованным желчными кислотами ингибированием функции клеток Панета [278]. Тем не менее, вторичные желчные кислоты, связанные с холецистэктомией, включая DCA, облегчали колит у мышей, ингибируя рекрутирование моноцитов/макрофагов [279]. Более того, УДХК может также снизить тяжесть колита, предотвращая потерю кластера Clostridium XIVa и увеличивая численность A. muciniphila [280]. Различные эффекты желчных кислот могут быть связаны с их химической структурой и потенциальными сопряженными фрагментами. Например, сульфатированные вторичные желчные кислоты могут оказывать более сильное провоспалительное действие по сравнению с их неконъюгированными аналогами, как это наблюдается у пациентов с воспалительными заболеваниями кишечника [281]. Конечно, необходимо более детальное метаболомическое профилирование, чтобы понять профиль желчных кислот у пациентов с ВЗК и определить про- или противовоспалительные эффекты каждого типа желчных кислот. В целом оказывается, что как SCFA, так и вторичные желчные кислоты обладают противовоспалительным действием в кишечнике (рис. 1A, B). В последние годы было идентифицировано несколько генов предрасположенности, повышающих риск развития ВЗК. Текущие исследования сосредоточены на идее о том, что генетическая предрасположенность, дисбиоз и факторы окружающей среды, такие как антибиотики, действуют совместно на развитие ВЗК. Белок 2, содержащий домен нуклеотидсвязывающей олигомеризации (NOD2, белок иммунологического внутриклеточного распознавания), идентифицирует внутриклеточный мурамилдипептид (MDP), неотъемлемый компонент бактериальных клеточных стенок [282]. Потеря функции NOD2 нарушает ингибирование TLR2-опосредованной активации NF-κB, что приводит к сверхактивному ответу Th1 и ослаблению иммунологической толерантности к микробам [282]. Кроме того, несколько других генов, которые повышают восприимчивость к ВЗК, включая связанный с аутофагией 16-подобный 1 (ATG16L1), белок 9, содержащий домен рекрутирования каспаз (Card9), и член A семейства 7 доменов лектинов C-типа (CLEC7A) , нарушают регуляцию Т-клеточных ответов и создают дисбактериоз кишечной микробиоты, что также способствует развитию ВЗК [283–285]. Будущие исследования должны выяснить, существуют ли однонуклеотидные полиморфизмы в генах, связанных с выработкой микробных метаболитов у пациентов с ВЗК.

Преимущества цистанхе трубчатой-укрепить иммунную систему
7.4. Колоректальная карцинома (КРР)
Растущий объем литературы предполагает роль микробиоты в развитии и прогрессировании рака. В сценариях, когда иммунная система развивается неадекватно, дисбактериоз кишечной микробиоты становится высоким риском, а распространение определенных микробов может привести к выработке мутагенных токсинов [286]. К этим генотоксинам относятся токсин Bacteroides fragilis (Bft), цитолетальный токсин, расширяющий структуру (CDT) и колибактин [225]. Однако они выделяют лишь небольшое количество токсинов, связанных с бактериями, и необходимы дополнительные исследования для выявления и понимания канцерогенного потенциала всех кишечных микробов [225]. Аденоматозные и зубчатые полипы представляют собой два предраковых поражения, которые часто перерастают в колоректальный рак (КРР). У пациентов с аденомами в кале увеличивается количество некоторых видов, включая Bilophila, Desulfovibrio, Mogibacterium и тип Bacteroidetes, тогда как у пациентов с зубчатыми полипами наблюдается увеличение таксонов Fusobacteria и класса Erysipelotrichia [226]. Fusobacterium nucleatum (F. nucleatum) характеризуется как важный микроб в прогрессировании CRC [287,288]. F. nucleatum способствует передаче сигналов TLR4 и передаче сигналов E-кадгерин/-катенин, что в конечном итоге приводит к активации NF-κB и снижению экспрессии miR-1322 [289]. Регуляторные микроРНК, такие как miR-1322, могут напрямую регулировать экспрессию CCL20, цитокина, который способствует метастазированию CRC [287]. Другая литература указывает на адгезин A F. nucleatum (FadA) как на ключевой фактор вирулентности, который позволяет F. nucleatum прикрепляться, инвазировать и разрушать эпителий толстой кишки [227]. Совсем недавно одно исследование показало, что F. nucleatum может способствовать развитию CRC, подавляя противоопухолевый иммунитет за счет активации ингибирующих рецепторов CEACAM1 и TIGIT1, которые подавляют NK-клетки и T-клетки [290]. Также было показано, что штамм F. nucleatum Fn7-1 усугубляет развитие CRC за счет повышения ответов Th17 [74]. Эти данные о F. nucleatum вызывают тревогу, поскольку это бактерия, продуцирующая SCFAs [291], а SCFA в целом рассматривались как потенциальное средство лечения многих воспалительных заболеваний. F. nucleatum преимущественно продуцирует ацетат и бутират, при этом недавно было высказано предположение, что F. nucleatum индуцирует Th17 через рецептор свободных жирных кислот 2 (FFAR2), рецептор SCFA [74]. Тем не менее, потеря FFAR2 у мышей усугубляла бактериальную нагрузку опухоли и чрезмерно активировала DC, что в конечном итоге способствовало истощению Т-клеток [292]. Более того, было обнаружено, что бутират из пищевых волокон менее метаболизируется в клетках CRC из-за эффекта Варбурга, что позволяет ему действовать как ингибитор HDAC и способствовать ацетилированию генов, связанных с апоптозом [293]. Эти данные подчеркивают, что патологические эффекты F. nucleatum могут быть независимыми от SCFA, но для определения этой возможности необходимы дальнейшие исследования. Другой предполагаемый механизм развития CRC предполагает, что чрезмерное потребление с пищей сахаров, белков и липидов может способствовать росту толерантных к желчи микробов, которые увеличивают выработку вторичных желчных кислот, таких как DCA и LCA, а также побочных продуктов. например, сероводород. Избыточное количество вторичных желчных кислот генотоксично и может создавать провоспалительную среду, которая может способствовать развитию КРР [226]. В частности, DCA может стимулировать канцерогенез в кишечнике путем активации зависимого от рецептора эпидермального фактора роста высвобождения металлопротеазы ADAM-17 [294].

последствия цистеина - лечите запор
DCA также активирует передачу сигналов -катенина [295] и запускает злокачественные трансформации в раковых стволовых клетках, экспрессирующих Lgr5- (Lgr5+) [296] для роста и инвазивности CRC. Однако количество бактерий, связанных с выработкой вторичных желчных кислот, то есть кластера Clostridium XlVa, было значительно уменьшено у пациентов с ВЗК, что сопровождалось снижением трансформации первичных желчных кислот во вторичные [297]. Помимо желчных кислот, кишечный микробный метаболит фолат может ухудшить патогенез CRC, запуская передачу сигналов AhR и повышая уровни Th17 [298]. Как и в случае с SCFA, необходимы дополнительные исследования, чтобы выявить потенциальные протуморогенные эффекты желчных кислот, полученных из кишечной микробиоты. При КРР наблюдаются отчетливые микробиот-зависимые иммунологические реакции. Что касается врожденных иммунных ответов, обогащение A. muciniphila способствовало поляризации макрофагов M1 NLRP3-зависимым образом, что подавляло онкогенез толстой кишки [299]. Аналогично, кишечная палочка, прикрепившаяся к кишечнику, может увеличивать количество макрофагов, продуцирующих IL-10-, что ограничивает воспаление кишечника и ограничивает образование опухолей [300]. Что касается адаптивного иммунитета, микробный дисбиоз гиперстимулирует CD8+ Т-клетки, что способствует хроническому воспалению и раннему истощению Т-клеток, что способствует восприимчивости к опухолям толстой кишки [301]. Раковые клетки кишечника также могут реагировать на микробиоту, индуцируя кальциневрин-зависимую секрецию IL-6, которая способствует опухолевой экспрессии коингибирующих молекул B7H3/B7H4, которые уменьшают противоопухолевые CD8+ Т-клетки [302]. Для сравнения, введение Helicobacter hepaticus индуцировало Т-фолликулярные хелперные клетки, которые восстанавливали противоопухолевый иммунитет на мышиной модели CRC [303]. По сравнению с макрофагами и клетками Th17, δ Т-клетки и резидентные Т-клетки памяти обнаруживались с более низкой частотой в ткани толстой кишки пациентов с КРР [60]. Было бы интересно выяснить, можно ли разработать панель иммунных клеток для ранней диагностики КРР.

цистанхе трубчатой – улучшает иммунную систему
7.5. Гепатоцеллюлярная карцинома (ГЦК)
Гепатоцеллюлярная карцинома (ГЦК), наиболее распространенный первичный рак печени, является четвертой по значимости причиной смертности от рака во всем мире [304]. Основная этиология патогенеза ГЦК связана с ранее существовавшими заболеваниями печени, такими как неалкогольная жировая болезнь печени (НАЖБП) и стеатогепатит, которые приводят к циррозу печени [305]. Ситуация еще более осложняется другими сопутствующими заболеваниями у пациентов с НАЖБП, включая резистентность к инсулину, ожирение и метаболические нарушения, которые еще больше способствуют воспалению печени и онкогенезу посредством IL-6 и TNF- [306]. Печень является «первой остановкой» для венозной крови, поступающей из кишечника, что делает ее уязвимой для микробиоты кишечника посредством транслокации микробов через кишечно-эпителиальный барьер или контакта с абсорбированными микробными метаболитами [307]. Вышеупомянутые хорошо известные эффекты дисбактериоза кишечной микробиоты, включая нарушение кишечного барьера, транслокацию микробов в кровоток и последующие воспалительные иммунные реакции посредством индукции PRR с помощью PAMP, таких как LPS, тесно коррелируют с патогенезом НАЖБП. цирроз печени и ГЦК [228,307]. Хотя долгое время считалось, что дисбактериоз кишечной микробиоты предшествует развитию ГЦК, эта причинно-следственная связь не изучалась глубоко до недавнего времени. Бехари, Рапозо и др. недавно обнаружено, еще до прогрессирования ГЦК, что дисбактериоз кишечной микробиоты сочетается с ранним поражением печени, за которым следует ЛПС-зависимый Th1- и Th17--опосредованный цитокиновый ответ [308]. Дальнейшие исследования должны определить, является ли дисбактериоз кишечной микробиоты причиной или следствием повреждения печени, предшествующего ГЦК. У пациентов с НАЖБП-ассоциированной ГЦК было отмечено увеличение количества Enterobacteriaceae и Streptococcus и снижение количества Akkermansia, наряду с повышенными уровнями медиаторов воспаления, таких как CCL3, CCL4, CCL5, IL-8 и IL-13. 309]. Более недавнее исследование выявило снижение численности бактерий, продуцирующих SCFA, и увеличение количества бактерий, продуцирующих ЛПС, у пациентов с ГЦК, индуцированной циррозом печени, но не выявило существенных признаков дисбиоза кишечной микробиоты при других заболеваниях печени, таких как гепатит С, гепатит В или алкогольная зависимость печени. болезнь [310]. Однако в целом следует отметить, что измененные микробные популяции, наблюдаемые в ходе многочисленных исследований, не согласуются друг с другом [309,311–313]. Более того, хотя обычно считается, что КЦЖК, продуцируемые кишечными микробами, имеют ряд преимуществ для человека, недавно было обнаружено, что инулин, предшественник бутирата КЦЖК, может способствовать прогрессированию ГЦК у генетически измененных дисбиотических мышей [229]. Другие исследования были сосредоточены на влиянии микробных метаболитов на ГЦК. Например, диета с высоким содержанием жиров привела к чрезмерному росту в кишечнике грамположительных организмов, которые генерируют вторичные желчные кислоты, то есть DCA [230]. DCA может работать совместно с липотейхоевой кислотой, активируя TLR2 и впоследствии подавляя противоопухолевый иммунитет, создавая микроокружение, благоприятное для развития ГЦК [314,315]. В целом, похоже, что метаболиты кишечной микробиоты потенциально являются проопухолевыми для печени.
7.6. Сердечно-сосудистые заболевания
Сердечно-сосудистые заболевания (ССЗ) тесно связаны с метаболическим синдромом, состоянием, которое включает в себя ряд взаимосвязанных заболеваний — в основном атеросклероз, НАЖБП, гипертонию и сахарный диабет II типа (TIIDM), — которые возникают в результате хронического, вялотекущего воспаления [316] . Многие клетки с высокой метаболической активностью, такие как паренхиматозные клетки печени и поджелудочной железы, адипоциты и скелетные миоциты, участвуют в обширных перекрестных взаимодействиях с иммунными клетками. Любое нарушение микробиома потенциально может изменить иммунную функцию хозяина и, как следствие, может вызывать или изменять болезненные процессы в метаболически активных тканях. Считается, что распознавание ЛПС и других микробных PAMP с помощью PRR является ключевым фактором в этом воспалительном состоянии низкой степени тяжести [231]. Также отмечено, что N-оксид триметиламина (ТМАО), микробный кометаболит, вызывает слабое воспаление посредством передачи сигналов NF-κB, активации воспаления и увеличения производства свободных радикалов [317,318]. Кроме того, ТМАО приводит к атеросклерозу и, следовательно, к болезням сердца, нарушая метаболизм холестерина в макрофагах и способствуя образованию пенистых клеток [319]. Действительно, более высокий уровень ТМАО в сыворотке коррелирует с повышенным риском атеросклероза, ишемической болезни сердца, инсульта и воспаления сосудов [232,233], а ТМАО в настоящее время рассматривается как биомаркер неблагоприятных сердечно-сосудистых событий [320]. Более поздние исследования обнаружили фенилацетилглутамин (PAGln) как микробный метаболит, связанный с сердечно-сосудистыми заболеваниями посредством активации адренергических рецепторов и протромботических эффектов [321,322]. Существует множество потенциальных новых ролей PAGln в сердечно-сосудистой медицине, например, его использование в качестве диагностического маркера или даже в качестве предиктора чувствительности к терапии β-блокаторами у пациентов с сердечно-сосудистыми заболеваниями [322].
7.7. Диабет
Сахарный диабет — это заболевание, разделенное на два класса: сахарный диабет I типа (TIDM) включает аутоиммунное разрушение островковых клеток поджелудочной железы, а сахарный диабет II типа (TIIDM) включает приобретенную нечувствительность к инсулину. Хотя многие исследования, связанные с микробиотой и диабетом, вращаются вокруг TIIDM и ожирения, было показано, что увеличение потребления SCFA с пищей может привести к изменению микробиоты и различным иммунным профилям у пациентов с TIDM [323]. Также было показано, что увеличение содержания в рационе SCFAs, таких как бутират и ацетат, действует синергически, обеспечивая защиту от популяций аутореактивных Т-клеток и TIDM у мышей [100]. Для сравнения, введение Parabacteroides distasonis ускорило развитие СД1 на мышиной модели, и это произошло из-за аберрантных иммунных реакций, включая повышение CD8+ Т-клеток и снижение Foxp3+ CD4+ Treg. клетки [324]. Следует отметить, что нарушение регуляции метаболизма желчных кислот является потенциальным предрасполагающим фактором островкового аутоиммунитета и диабета 1 типа [325]. Микробиом и иммунная система активно участвуют в патогенезе TIIDM. Аминокислоты с разветвленной цепью продуцируются Prevotella copri (P. copri) и Bacteroides vulgatus spp., а P. copri непосредственно индуцирует резистентность к инсулину у мышей [326,327]. Истощение комменсального A. muciniphila нарушает кишечный барьер, что приводит к транслокации эндотоксина в кровоток и последующей активации моноцитов CCR2+. Это приводит к превращению клеток B1a поджелудочной железы в клетки 4BL, которые высвобождают медиаторы воспаления и вызывают обратимую или необратимую резистентность к инсулину [328]. С другой стороны, микробные метаболиты, такие как линолевая кислота и докозагексаеновая кислота, обладают защитным действием против инсулинорезистентности и TIIDM посредством противовоспалительного действия и предотвращения липотоксичности [329]. Также было показано, что FMT снижает уровень глюкозы в крови натощак и снижает резистентность к инсулину у мышей с TIIDM [330]. Более того, некоторые терапевтические эффекты некоторых противодиабетических препаратов могут быть частично обусловлены их способностью изменять микробиоту [331–333].
7.8. Гипертония
В нескольких исследованиях наблюдались значительные изменения в составе микробиома у мышей с нормальным и гипертоническим давлением, хотя специфические микробные профили у мышей с гипертонией зависят от используемой модели гипертензии [334–337]. В модели гипертонии, связанной с ангиотензином II, отсутствие микробиоты у стерильных мышей защищает от гипертонии частично за счет уменьшения популяций воспалительных клеток в крови [338]. Тем не менее, стерильные мыши были более склонны к повреждению почек после комбинированного режима ангиотензина II и диеты с высоким содержанием соли [339]. Более того, повторное введение микробиоты гипотензивным мышам без микробов восстановило сократимость сосудов [340]. Как правило, состав микробиоты у гипертонических и нормотензивных животных различается, и, что интересно, перекрестное вскармливание детенышей с гипертонической болезнью и нормотензивных самок может снизить кровяное давление в первой группе [341]. Подобно сердечно-сосудистым заболеваниям, кишечный метаболит ТМАО также имеет отношение к гипертонии. Недавнее исследование показало, что ТМАО усугубляет вазоконстрикцию через АФК у мышей с гипертензией, индуцированной ангиотензином II [342]. Аналогично, активация ДК, вызванная высоким содержанием соли, связана с гипертензией, опосредованной микробным дисбактериозом [343]. Для сравнения, содержание кетоновых тел -гидроксибутират снижается у крыс с гипертонией, получавших пищу с высоким содержанием соли; Спасение с помощью предшественника -гидроксибутирата 1,3-бутандиола снизило кровяное давление и воспаление почек за счет предотвращения воспаления, опосредованного NLRP3- [344]. Хотя в других исследованиях было показано, что HSD снижает количество Lactobacillus spp. и индуцируют популяции клеток Th17, по-видимому, это происходит по совершенно другому механизму [176].
7.9. Ревматоидный артрит
Становится все более понятным патогенез ревматоидного артрита (РА) — системного аутоиммунного заболевания, характеризующегося преимущественно воспалением суставов. РА является многофакторным заболеванием с множественными идентифицированными аллелями и факторами окружающей среды, обуславливающими повышенную восприимчивость к этому заболеванию. Потенциально важным микробным родом в развитии РА является Prevotella. Впервые это было выявлено в 2013 году Шером и др., которые обнаружили, что у пациентов с впервые возникшим РА значительно увеличилась численность видов Prevotella, особенно Prevotella copri, по сравнению со здоровыми людьми из контрольной группы [234]. Однако популяция Prevotella не увеличивалась у пациентов с хроническим РА [234]. С тех пор многочисленные исследования обнаружили дальнейшую корреляцию между различными видами Prevotella и РА [345–347]. Однако неясно, являются ли Prevotella spp. сам по себе способствует патогенезу РА, или иммунологическая среда, создаваемая РА, увеличивает численность Prevotella в кишечнике. Другие заметные бактериальные сдвиги в микробиоте кишечника у пациентов с РА включают цветение протеобактерий, кластера Clostridium XlVa и Ruminococcus, что коррелирует с меньшим количеством CD4+ T-клеток и Treg-клеток [348]. Используя модель аутоиммунного артрита K/BxN, было обнаружено, что SFB-опосредованное снижение цитотоксического Т-лимфоцитарного антигена-4 (CTLA-4) вызывает аутореактивные Т-фолликулярные хелперные клетки [349,350]. Накопление Т-фолликулярных хелперных клеток и клеток Th17 при артрите, по-видимому, зависит от возраста [351], что помогает объяснить, почему РА обнаруживается преимущественно у пожилых людей. Однако интересно, что микробиота кишечника, по-видимому, преимущественно влияет на Т-фолликулярные хелперные клетки, а не на клетки Th17, что подтверждено лечением антибиотиками на модели аутоиммунного артрита K/BxN [352]. Следует отметить, что недавно сообщалось, что коллаген-индуцированный РА у мышей вызывает аберрантность циркадных ритмических паттернов в микробиоме кишечника, что приводит к снижению целостности барьера из-за изменения циркулирующих факторов микробного происхождения, таких как метаболиты триптофана [353]. SCFAs, в частности бутират, были предложены в качестве варианта лечения РА. Было обнаружено, что добавки бутирата способствуют развитию Treg-клеток путем ингибирования экспрессии HDAC и подавляют гены провоспалительных цитокинов при РА [354]. Более того, бутират облегчал артрит, непосредственно индуцируя дифференцировку функциональных фолликулярных Treg-клеток in vitro путем усиления ацетилирования гистонов посредством ингибирования HDAC [355]. Кроме того, бутират уменьшал тяжесть артрита за счет увеличения уровней лигандов AhR, то есть метаболита серотонина 5-гидроксииндол-3-уксусной кислоты, где активация AhR поддерживает регуляторную функцию B-клеток [356]. Совсем недавно было обнаружено, что помимо SCFA, метаболиты, полученные из кишечной микробиоты, LCA, DCA, isoLCA и 3-oxoLCA, обладают противоартритным действием. В частности, isoLCA и 3-oxoLCA ингибировали дифференцировку Th17 и способствовали поляризации макрофагов M2 [357]. Эти эффекты вторичных желчных кислот могут быть усилены добавлением пробиотиков Parabacteroides distasonis [357]. Новые данные о вторичных желчных кислотах являются монументальными и требуют дополнительных исследований.

цистанхе трубчатой – улучшает иммунную систему
Нажмите здесь, чтобы просмотреть продукты Cistanche Enhance Immunity
【Запросить дополнительную информацию】 Электронная почта:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
7.10. Аллергические заболевания
Аллергия возникает, когда иммунная система становится гиперчувствительной к непатогенным чужеродным антигенам. К частым проявлениям гиперчувствительности относятся аллергический ринит, пищевая аллергия, экзема, атопический дерматит и астма. Некоторые факторы, ответственные за развитие аллергии, такие как снижение микробного воздействия, кесарево сечение, диета и использование антибиотиков, тесно связаны с изменениями в составе микробиома кишечника [358–361]. Дисбактериоз кишечной микробиоты, в свою очередь, увеличивает риск аллергии, особенно пищевой аллергии [235,236]. Дисбиоза, вызванного применением антибиотиков, достаточно, чтобы усилить аллергические симптомы, усилить воспаление кишечника и нарушить плотный контакт слизистой оболочки кишечника у сенсибилизированных мышей [362]. Диета с высоким содержанием жиров обычно имеет эффекты, аналогичные эффектам антибиотиков, вызывая дисбактериоз кишечной микробиоты и впоследствии увеличивая риск пищевой аллергии [363]. Изменения в составе микробиоты кишечника сразу после рождения, когда микробиом еще сформирован, по-видимому, оказывают особенно большое влияние на развитие аллергических заболеваний в более позднем возрасте [364]. Следует отметить, что вагинальная микробиота также может отражать риск аллергии, при этом кластеры вагинальной микробиоты с преобладанием лактобацилл были связаны со статусом IgE в сыворотке младенцев в возрасте 1 года [365]. Некоторые исследования подтверждают концепцию о том, что дисбактериоз тесно связан с аллергическими заболеваниями, особенно с астмой. У лиц с атопической астмой уровень Lactobacillus и E. coli в фекалиях значительно выше, чем у здоровых людей [366]. Что касается метаболитов микробиоты, 12,13-diHOME (относительно неизведанная линолевая кислота) обычно обнаруживается у новорожденных с высоким риском развития астмы [367]. Недавно было обнаружено, что бактериальная эпоксидгидролаза, которая продуцирует 12,13-diHOME, также имеет более высокую концентрацию во время воспаления легких, а 12,13-diHOME восстанавливает клетки Treg в легких [368,369]. Для сравнения, лиганд AhR тетрахлордибензо-п-диоксин был способен ослаблять гиперчувствительность замедленного типа, индуцируя клетки Treg, подавляя клетки Th17 и обращая вспять дисбиоз микробиоты кишечника [370]. Аналогичным образом, у людей с более высоким содержанием КЖК в фекалиях, таких как бутират и пропионат, в раннем возрасте заметно снизился риск развития астмы и атопии [371]. Имея потенциальную терапевтическую ценность, добавление SCFA может модулировать Т-клетки и DC для облегчения астмы [372]. Аналогичным образом было показано, что добавление матерью пищевых волокон или ацетата защищает новорожденных от астмы, способствуя ацетилированию гена Foxp3 [373]. Кормление пищевыми волокнами также обеспечивало защиту от пищевых аллергенов за счет активности дегидрогеназы сетчатки в CD103+ DCs [374]. Следует отметить, что недавно было обнаружено, что пищевая клетчатка инулин способствует развитию воспаления 2 типа, вызванного аллергенами и гельминтами, и это зависит от желчных кислот [375]. В целом оказывается, что влияние микробиоты кишечника на аллергию в значительной степени регулируется метаболитами, но каждый микробный продукт имеет независимые эффекты, которые могут либо способствовать, либо снижать гиперчувствительность.
7.11. Психические расстройства: ось кишечник-мозг
Вышеупомянутая информация описывает влияние кишечной микробиоты как на внутрикишечные, так и на внекишечные заболевания. Еще одним органом, на который может влиять микробиота кишечника, является мозг, где «напряженный кишечник» все чаще признается патологическим образованием при некоторых неврологических расстройствах. У недоношенных детей с незрелой кишечной микробиотой избыточный рост клебсиелл является высокопрогностическим фактором повреждения головного мозга и связан с провоспалительным иммунологическим тонусом [376]. Болезнь Паркинсона характеризуется накоплением альфа-синуклеина в кишечнике, и пациенты часто страдают от синдрома повышенной проницаемости кишечника из-за дисбиоза микробиоты с более высокими популяциями Prevotellaceae [13]. Эти симптомы можно обратить вспять путем приема пробиотиков [377,378]. В последнее время идея о том, что микробиота влияет на психическое здоровье, начала набирать обороты. Таксономические и метаболические признаки были предложены в качестве биомаркеров для разделения большого депрессивного расстройства на категории легких, умеренных и тяжелых симптомов [379]. Несколько исследований, изучающих различия в микробиоте между психически здоровыми людьми и людьми с психическими расстройствами, такими как тревога и/или депрессия, показали, что микробная колонизация до и после рождения играет важную роль в дальнейшей жизни. Например, материнский стресс может вызвать аномальное развитие нервной системы у потомства, что отмечено значительным снижением количества Bifidobacterium spp. [380]. Более того, новорожденные, родившиеся с помощью кесарева сечения, в отличие от вагинальных родов, имеют больший риск развития психоза в более позднем возрасте [377,381]. Впечатляет то, что лечение окситоцином в раннем возрасте может минимизировать нарушения поведения, наблюдаемые у щенков, родившихся с помощью кесарева сечения [382]. Коктейль антибиотиков широкого спектра действия, разрушающих кишечную микробиоту, особенно на постнатальном этапе и на этапе отлучения от груди, может вызывать долгосрочные последствия связанных с тревогой поведенческих последствий в подростковом и взрослом возрасте [383]. Недавнее элегантное исследование Li et al. установили, что воздействие антибиотиков на младенцев приводило к тревожно-депрессивному поведению и нарушениям памяти, которые сопровождались усилением воспалительной среды; аналогичные результаты были получены после длительного лечения антибиотиками на подростковой и взрослой стадии у мышей [384]. Нарушение микробиоты кишечника в раннем возрасте также может вызывать тревожное поведение, специфичное для пола, при этом лечение ЛПС у крыс Вистар приводило к меньшему социальному взаимодействию у самцов по сравнению с самками, у которых наблюдалось усиление социального поведения [385]. Примечательно, что FMT от «старого микробиома» до стерильных мышей снижал содержание SCFAs, и это было связано со снижением когнитивных функций [386]. Ось кишечная микробиота-иммунитет-мозг все еще находится в зачаточном состоянии и требует исследования для установления механизмов, участвующих в иммунной регуляции, ответственных за поведенческие аномалии и неврологические расстройства. Однако необходимо обратить внимание на другие микроорганизмы, помимо бактерий, поскольку было обнаружено, что грибы слизистых оболочек способствуют социальному поведению посредством дополнительных иммунных механизмов Th17 [387].
8. Связь между микробиотой кишечника и их метаболитами в иммунотерапии.
В настоящее время передовые методы иммунотерапии включают Т-клетки (ингибиторы контрольных точек, агонисты костимулирующих рецепторов), модификацию Т-клеток, адоптивный перенос Т-клеток, аутологичные цитокин-индуцированные клетки-киллеры, терапию химерными антигенными рецепторами, цитокины, онколитические вирусы и вакцины [388,389]. В последние годы иммунотерапия основана на применении ингибиторов иммунных контрольных точек (ICI), включая антитела против CTLA-4, белка программируемой гибели клеток 1 (PD-1) и лиганда программируемой смерти 1 (PD-L1). ), был одобрен в качестве лечения первой или второй линии при различных опухолях [390]. В частности, ICI, нацеленные на PD-1 и его лиганд PD-L1, были одобрены Управлением по контролю за продуктами и лекарствами США (FDA) для лечения 10 различных типов рака [391]. Недавние исследования показывают, что микробиота кишечника может быть важным фактором, определяющим ответ на иммунотерапию рака в некоторых доклинических и клинических исследованиях [392–394]. Мэтсон и др. показали, что Bifidobacterium longum, Collinsella aerofaciens и Enterococcus faecium имеют более высокую численность у пациентов, реагирующих на ингибиторы PD-1 [395]. В нескольких исследованиях были обнаружены значительные различия в микробиомах ответивших и не ответивших на ингибиторы PD-1, включая увеличение количества Faecalibacterium, Ruminococcus и Akkermansia у ответивших и увеличение количества Bacteroides у неответивших [392,396,397]. Кроме того, лечение анти-PD-1 пациентов с раком печени приводило к увеличению численности Faecalibacterium и лучшей выживаемости без прогрессирования [398]. Дополнительные исследования также показали, что состав кишечных бактерий может влиять на метаболизм некоторых иммунотерапевтических препаратов. Перенос фекалий от пациентов, получавших лечение PD-1-, реагирующих на лечение, мышам, свободным от микробов, усиливал Т-клеточные реакции и повышал эффективность терапии ингибиторами PD-1 [395]. Инозин, который продуцируется Bifidobacterium pseudolongum и Akkermansia muciniphila, также способствует терапии анти-CTLA-4 и анти-PD-L1 путем активации Т-клеток [213]. Для сравнения, недавнее исследование Coutzac et al. показали, что бутират и пропионат ограничивают эффективность ингибиторов CTLA-4, что связано с более высокой популяцией Treg и более низкой выживаемостью [399]. Следует отметить, что недавно выделенный пробиотический штамм Lactobacillus (L. paracasei sh2020) способствовал анти-PD-1 эффектам у мышей с опухолями CRC путем повышения экспрессии CXCL10 в опухолях и последующего усиления CD8+ T. рекрутирование клеток [400]. Примечательно, что эти противоопухолевые эффекты наблюдались даже при наличии дисбактериоза кишечной микробиоты. Эти доклинические и клинические данные подтверждают продолжение исследований с целью определить необходимость кишечной микробиоты для обеспечения максимальной эффективности иммунотерапии (рис. 3). Это включает в себя, возможно, использование кишечной микробиоты для ограничения негативных побочных эффектов иммунотерапии, таких как кардиотоксичность, связанная с ICI. Чен и др. элегантно описанный ингибитор PD-1/PD-L1 для истощения популяций микробиоты Prevotellaceae и Rikenellaceae, снижения уровня бутирата и стимулирования провоспалительной поляризации макрофагов M1 посредством подавления оси PPAR-CYP4 × 1 [401]. Что касается терапевтической значимости, реколонизация Prevotella loescheii и добавление бутирата облегчали кардиотоксичность, связанную с ингибитором PD-1/PD-L1 [401]. Поскольку иммунные контрольные точки часто неоднородны и непостоянны, что может привести к снижению эффективности лечения, устойчивости к лекарствам и побочным реакциям [402–404], терапия, нацеленная на кишечную микробиоту, может быть важным адъювантом (рис. 3). В настоящее время одобренными и доступными методами лечения воспалительного заболевания кишечника являются агенты против TNF, агенты против интегрина, моноклональные антитела против - 7 и ингибиторы янус-киназы (JAK). Ингибиторы JAK (например, барицитиниб) успешно восстанавливали передачу сигналов инсулина и улучшали миостеатоз после кормления с высоким содержанием жиров и сахара, но они не обращали вспять вызванные диетой изменения в микробиоте кишечника у мышей [405]. Ингибиторы анти-ФНО улучшили клинические результаты как при БК, так и при ЯК, но они по-прежнему требуют более рандомизированных клинических исследований [402]. Однако примечательно, что недавно было обнаружено, что FMT является потенциальной альтернативной терапией для пациентов с БК с предшествующей потерей ответа или непереносимостью терапии анти-TNF (т.е. инфликсимаба) [406]. Впечатляюще, что пробиотик Bifidobacterium longum (B. longum) CECT 7894 способствовал повышению эффективности инфликсимаба на модели колита у мышей за счет уменьшения количества условно-патогенных микроорганизмов, т.е. Enterococcus и Pseudomonas, и увеличения количества вторичных желчных кислот [407]. Другое недавнее исследование аналогичным образом показало, что терапия как анти-TNF, так и анти-IL-12/23 изменяет микробиоту кишечника, отдавая предпочтение видам микробов, способным к вторичной выработке желчных кислот [408]. Повышение уровня вторичных желчных кислот может быть связано с лечением анти-ФНО, способствующим цветению Clostridia spp. в рамках восстановления микробиоты кишечника [409]. Желчные кислоты считаются потенциальным метаболическим биомаркером ответа на терапию анти-TNF [410], но необходимы дополнительные исследования, чтобы определить, улучшают ли желчные кислоты эффективность иммунотерапии (рис. 3). Есть намек на то, что вторичные желчные кислоты могут быть полезны при рассмотрении доказательств эффективности лечения УДХК для предотвращения повторного возникновения КРР путем ингибирования передачи сигналов NF-κB [411,412]. Более того, было обнаружено, что УДХК взаимодействует с эффектами анти-PD1, ингибируя прогрессирование рака у мышей с опухолями [413]. В целом, похоже, что микробиота кишечника может использоваться как в качестве биомаркера, так и в качестве терапевтической мишени для улучшения ответа на иммунотерапию.
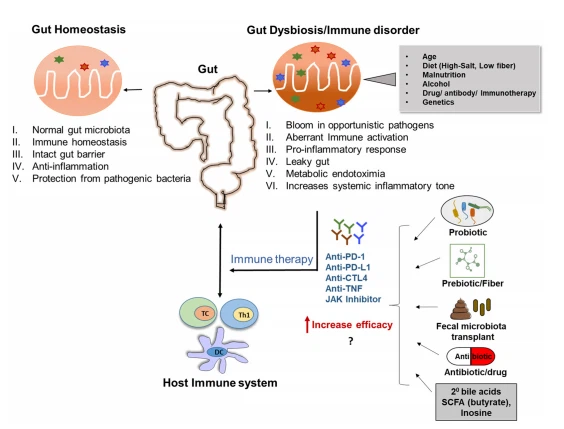
Рисунок 3. Изменение численности популяции кишечной микробиоты может повлиять на результаты иммунотерапии. Здоровый микробиом кишечника может повысить биодоступность и эффективность лекарств у хозяина. Дисбактериоз, вызванный несколькими описанными факторами, может снизить эффективность терапевтических препаратов, что приведет к плохим терапевтическим результатам. Изменение микробиоты кишечника может повысить эффективность некоторых иммунотерапевтических препаратов, таких как антитела против PD-1, антитела против PD-L1 и лечение антителами против CTL4. Микробиоту кишечника можно изменить путем добавления антибиотиков, пробиотиков, пребиотиков, вторичных желчных кислот, короткоцепочечных жирных кислот (например, бутирата), инозина или трансплантации фекалий.
9. Перспективы, проблемы и риски в исследованиях иммунитета и микробиома.
Взаимодействие между микробиотой и иммунной системой и их влияние на заболевания, включая воспалительные заболевания кишечника, аутоиммунный артрит и рак, невероятно сложны. Один уровень сложности включает в себя задачу показать точное влияние определенной отдельной бактерии или группы бактерий на возникновение заболевания или общую физиологию хозяина. Колонизация микробов на безмикробных моделях является актуальной стратегией, позволяющей лучше понять потенциальное влияние кишечных микроорганизмов на здоровье и болезни хозяина [414]. Однако микробиота кишечника — это гораздо больше, чем просто несколько избранных видов. В среде микробиома наблюдается сильная динамика, где виды либо взаимоисключают друг друга, либо конкурируют за ресурсы, а рост многих микробов зависит друг от друга [415]. Другой уровень сложности включает в себя другие взаимодействующие генетические факторы и факторы окружающей среды, такие как диета, курение, наркотики и лекарства (рис. 2). Это включает в себя различия в микробиоте (и потенциально иммунных реакциях) между городскими и сельскими районами для отдельных людей [416]. Тем не менее, наблюдения, наблюдаемые на моделях грызунов, не всегда применимы к людям. В целом можно констатировать, что люди и другие млекопитающие живут в «более грязной» среде по сравнению с исследовательскими грызунами, живущими в специфических средах, свободных от патогенов. Следовательно, чистота окружающей среды, отражающая гигиеническую гипотезу, может влиять на состав микробиоты и восприимчивость к болезням. Это мнение подтверждается недавним открытием о том, что оплодотворенные мыши (животные, постоянно подвергающиеся воздействию среды типа скотного двора) имели более стабильную микробиоту кишечника и оставались устойчивыми к неоплазиям, вызванным мутагенами и колитом, по сравнению с мышами, рожденными в гигиенических условиях [417].
В нескольких исследованиях, посвященных исследованиям микробиома и иммунитета, для характеристики микробиома использовалось секвенирование 16S рРНК, но этот метод имеет ограничения, заключающиеся в том, что он может успешно идентифицировать роды, но не может обеспечить различия на уровне видов [418]. Поэтому для достижения более инклюзивного изучения микробиомов целесообразно сочетать метагеномику с другими подходами -омики [419]. В последнее время метатранскриптомика и метаболомика быстро становятся важными для исследований микробиома. Метагеномика генерирует таксономический профиль образца, метатранскриптомика получает функциональный профиль, а метаболомика завершает описание, определяя, какие побочные продукты высвобождаются микробиотой в окружающую среду [419]. Хотя каждый из этих подходов -омики сам по себе предоставляет ценную информацию, предполагается, что более полную картину дает комбинированная -омика. Одним из важных преимуществ этих подходов -omics является то, что необработанные файлы можно хранить в базах данных, а затем использовать для анализа другими исследовательскими группами. Одним из ограничений, которое может возникнуть при применении машинного обучения для сравнения нескольких баз данных, является неравномерность размера выборки [420]. Более того, результаты -омики можно считать специфичными для исследования, поскольку может быть трудно найти пересекающиеся закономерности изменений микробиоты кишечника между научными и/или клиническими исследованиями. Это связано с тем, что микробиота кишечника (плюс их метаболиты) и восприимчивость к заболеваниям могут различаться у людей в зависимости от их географического происхождения [421], и даже бактериальный состав у обычных лабораторных грызунов может различаться в зависимости от исследовательских учреждений и поставщиков [422]. В целом, -омика, несомненно, продвигает биомедицинскую область для определения потенциальных диагностических и терапевтических целей, но все еще существуют некоторые ограничения, которые необходимо преодолеть.
10. Выводы
Таким образом, иммунная система хозяина и микробиом кишечника во многом зависят друг от друга в плане нормального функционирования и благополучия хозяина (подведено в графическом описании). В этом обзоре были рассмотрены новые результаты, в том числе то, как иммунная подготовка плода экологически зависит от микробиоты матери (здоровая, дисбактериозная или стрессовая). Обсуждались новые механизмы механизма, такие как SCFA и вторичные желчные кислоты, модулирующие гомеостаз кишечника путем индуцирования Treg-клеток и секреции IL-10 (рис. 1A, B). На протяжении всего обзора неоднократно упоминалось, что бутират и его пищевые волокна-предшественники влияют на иммунные реакции и действуют как потенциальные терапевтические средства при многих заболеваниях, но некоторые данные свидетельствуют о том, что их клиническую практику, возможно, необходимо учитывать в контексте заболевания. Для сравнения, пробиотики и FMT кажутся более многообещающими в восстановлении эубиотиков кишечной микробиоты и облегчении воспалительных заболеваний. Более того, микробиота кишечника, по-видимому, является актуальной целью для улучшения современных иммунотерапевтических методов и уменьшения их негативных побочных эффектов (рис. 3). Мы также обсудили текущие проблемы в исследованиях микробиома, которые, по сути, основаны на генетических факторах и факторах окружающей среды (рис. 2), которые делают каждую микробиоту уникальной среди людей, а также при сравнении видовых моделей. Мы полагаем, что недавние разработки в области мультиомики, включая эпигеномику, метагеномику, метапротеомику, метаболомику, культуромику и одноклеточную транскриптомику, прояснят взаимодействие между микробиомом кишечника и иммунной системой в норме и при заболеваниях [423] . Таким образом, будет интересно предсказать «специфические» иммунные реакции хозяина на основе профилей кишечного микробиома, что будет способствовать разработке «персонализированной, нацеленной на микробиом» терапии иммунологических заболеваний.
Рекомендации
1. Донн Дж. Ни один человек не является островом; Иллюстрировано Полом Питером Пичем; Taurus Press: Уиллоу Дин, Великобритания, 1975.
2. Бим, А.; Клингер, Э.; Хао, Л. Влияние диеты и пищевых компонентов на состав микробиоты кишечника. Питательные вещества 2021, 13, 2795. [CrossRef] [PubMed]
3. Шанахан, Ф.; Гош, Т.С.; О0 Тул, П.В. Здоровый микробиом. Каково определение здорового кишечного микробиома? Гастроэнтерология 2021, 160, 483–494. [Перекрестная ссылка] [PubMed]
4. Вальдес А.М.; Уолтер, Дж.; Сигал, Э.; Спектор, Т.Д. Роль микробиоты кишечника в питании и здоровье. БМЖ 2018, 361, к2179. [Перекрестная ссылка] [PubMed]
5. Булл, М.Дж.; Пламмер, Северная Каролина. Часть 1: Микробиом кишечника человека в состоянии здоровья и болезней. Интегр. Мед. 2014, 13, 17–22.
6. Сакс Д.; Бакстер, Б.; Кэмпбелл, Британская Колумбия; Карпентер, Дж. С.; Коньяр, К.; Диппель, Д.; Иса, М.; Фишер, Ю.; Хаузеггер, К.; Хирш, Дж. А. Межобщественный консенсус по улучшению качества Пересмотренное консенсусное заявление по эндоваскулярной терапии острого ишемического инсульта. Межд. Дж. Инсульт 2018, 13, 612–632. [Перекрестная ссылка]
7. Матиясич, М.; Мештрович, Т.; Палетак, ХК; Перич, М.; Баресич, А.; Вербанак, Д. Микробиота кишечника за пределами бактерий-микобиома, вирома, археома и эукариотических паразитов при ВЗК. Инт Дж. Мол. наук. 2020, 21, 2668. [CrossRef]
8. Джуффре, М.; Кампиготто, М.; Кампишано, Г.; Комар, М.; Кроче, Л.С. История микробов печени и кишечника: как кишечная флора влияет на заболевания печени? Обзор литературы. Являюсь. Дж. Физиол. Гастроинтест. Физиол печени. 2020, 318, Г889–Г906. [Перекрестная ссылка]
9. Гомаа, Э.З. Микробиота/микробиом кишечника человека в здоровье и заболеваниях: обзор. Антони Ван Левенгук 2020, 113, 2019–2040 гг. [Перекрестная ссылка]
10. Миллс, С.; Стэнтон, К.; Лейн, Дж.А.; Смит, Дж.Дж.; Росс, Р.П. Точное питание и микробиом, Часть I: Современное состояние науки. Питательные вещества 2019, 11, 923. [CrossRef]
11. Адак А.; Хан, М.Р. Взгляд на микробиоту кишечника и ее функциональные возможности. Клетка. Мол. Наука о жизни. 2019, 76, 473–493. [Перекрестная ссылка]
12. Генсоллен Т.; Айер, СС; Каспер, Д.Л.; Блумберг, Р.С. Как колонизация микробиоты в раннем возрасте формирует иммунную систему. Наука 2016, 352, 539–544. [Перекрестная ссылка] [PubMed]
13. Джуффре, М.; Моретти, Р.; Кампишано, Г.; да Силвейра, ПРО; Монда, ВМ; Комар, М.; Ди Белла, С.; Антонелло, РМ; Луццати, Р.; Кроче, Л.С. Ты со мной разговариваешь? Говорит кишечная нервная система (ENS) микробу. Как кишечные микробы взаимодействуют с ЭНС. Дж. Клин. Мед. 2020, 9, 3705. [CrossRef]
14. Чо, Ю.; Шор, С.А. Ожирение, астма и микробиом. Физиология 2016, 31, 108–116. [Перекрестная ссылка] [PubMed]
15. МакКомб, С.; Тириот, А.; Акаче, Б.; Кришнан, Л.; Старк, Ф. Введение в иммунную систему. Методы Мол. Биол. 2019, 2024, 1–24. [Перекрестная ссылка] [PubMed]
16. Чан, Л.; Карими, Н.; Моровати, С.; Ализаде, К.; Какиш, Дж. Э.; Вандеркамп, С.; Фазель, Ф.; Наполеони, К.; Ализаде, К.; Мехрани, Ю.; и другие. Роль нейтрофилов в цитокиновых бурях. Вирусы 2021, 13, 2318. [CrossRef]
17. Домингес-Белло, МГ; Костелло, ЕК; Контрерас, М.; Магрис, М.; Идальго, Г.; Фирер, Н.; Найт, Р. Режим доставки формирует приобретение и структуру начальной микробиоты во многих средах обитания тела новорожденных. Учеб. Натл. акад. наук. США 2010, 107, 11971–11975. [Перекрестная ссылка]
18. Митчелл, СМ; Маццони, К.; Хогстром, Л.; Брайант, А.; Бергерат, А.; Шер, А.; Почан, С.; Герман, П.; Кэрриган, М.; Шарп, К.; и другие. Способ доставки влияет на стабильность микробиоты кишечника раннего возраста. Представитель Cell Med. 2020, 1, 100156. [CrossRef]
19. Сельма-Ройо, М.; Калатаюд Арройо, М.; Гарсия-Мантрана, И.; Парра-Льорка, А.; Эскьюриет, Р.; Мартинес-Коста, К.; Колладо, MC Перинатальная среда влияет на колонизацию микробиоты и рост ребенка: влияние на реакцию хозяина и функцию кишечника. Микробиом 2020, 8, 167. [CrossRef]
20. Субраманиан С.; Гэн, Х.; Ду, К.; Чжоу, премьер-министр; Бу, ВЧ; Ван, X.; Сваминатан, С.; Тан, Южная Каролина; Ридлон, Дж. М.; Де План, И.Г.; и другие. Режим кормления влияет на динамические характеристики микробиоты кишечника и влияет на восприимчивость к повреждению кишечника, вызванному моноклональными антителами к CD3, у новорожденных мышей. Являюсь. Дж. Физиол. Гастроинтест. Физиол печени. 2022, 323, G205–G218. [Перекрестная ссылка]
21. Вампач, Л.; Хайнц-Бушарт, А.; Фриц, СП; Рамиро-Гарсия, Дж.; Хабье, Дж.; Герольд, М.; Нараянасами, С.; Кайсен, А.; Хоган, АХ; Биндл, Л.; и другие. Способ рождения связан с самыми ранними функциями микробиома кишечника, обусловленными штаммом, и иммуностимулирующим потенциалом. Нат. Коммун. 2018, 9, 5091. [CrossRef] 22. Неги, С.; Хашимото-Хилл, С.; Аленгат, Т. Взаимодействие неонатальной микробиоты и эпителия, влияющее на инфекцию. Передний. Микробиол. 2022, 13, 955051. [CrossRef] [PubMed]
23. Сенн, В.; Басслер, Д.; Чоудри, Р.; Шолькманн, Ф.; Ригини-Грюндер, Ф.; Вуй-Дит-Биле, RN; Рестин, Т. Микробная колонизация от плода до раннего детства – комплексный обзор. Передний. Клетка. Заразить. Микробиол. 2020, 10, 573735. [CrossRef] [PubMed]
24. Ракайтете, Э.; Халкиас, Дж.; Фукуи, EM; Мендоса, В.Ф.; Хейзелден, К.; Кроуфорд, Эд; Фудзимура, Кентукки; Берт, Т.Д.; Линч С.В. Жизнеспособная бактериальная колонизация в кишечнике человека в период внутриутробного развития сильно ограничена. Нат. Мед. 2020, 26, 599–607. [Перекрестная ссылка]
25. Ли, Ю.; Зубакер, Дж. М.; Бен-Симон, С.; Озери, Л.; Швейцер, Р.; МакКорт, Британская Колумбия; МакКорт, CC; Вернер, Л.; Снаппер, SB; Шуваль, Д.С.; и другие. Внутриутробно кишечник человека содержит уникальный метаболом, включая бактериальные метаболиты. JCI Insight 2020, 5, e138751. [Перекрестная ссылка] [PubMed]
26. Джайн, Н. Образование иммунной системы в раннем возрасте: мамы, микробы и (упущенные) возможности. Кишечные микробы 2020, 12, 1824564. [CrossRef]
27. Геринская М.; Шульц-Дабровска, Л.; Струзик Дж.; Мельчарска, МБ; Грегорчик-Збороч, К.П. Целостность кишечного барьера: участие эпителиальных клеток и микробиоты - взаимные отношения. Животные 2022, 12, 145. [CrossRef]
28. Вестром, Б.; Аревало Суреда, Э.; Пьержиновска, К.; Пьержиновский, С.Г.; Перес-Кано, Ф.Дж. Незрелый кишечный барьер и его значение в установлении иммунитета у новорожденных млекопитающих. Передний. Иммунол. 2020, 11, 1153. [CrossRef]
29. Рабе, Х.; Лунделл, AC; Сьоберг, Ф.; Люнг, А.; Стромбек, А.; Гио-Батта, М.; Маглио, К.; Нордстрем, И.; Андерссон, К.; Нукаев, И.; и другие. Колонизация кишечника новорожденного бифидобактериями связана с более высокими цитокиновыми реакциями у детей. Кишечные микробы 2020, 12, 1847628. [CrossRef]
30. Хенрик, Б.М.; Родригес, Л.; Лакшмикант, Т.; Поу, К.; Хенкель, Э.; Арзооманд, А.; Олин, А.; Ван, Дж.; Майкс, Дж.; Тан, З.; и другие. Импринтинг иммунной системы, опосредованный бифидобактериями, в раннем возрасте. Ячейка 2021, 184, 3884–3898. [Перекрестная ссылка]
31. Чин, Н.; Мендес-Лагарес, Г.; Тафт, Д.Х.; Лало, В.; Киу, Х.; Нараян, Северная Каролина; Робертс, С.Б.; Миллс, Д.А.; Хартиган-О0 Коннор, диджей; Флаерман, В.Дж. Временное влияние добавок детского питания на кишечную микробиоту. Питательные вещества 2021, 13, 807. [CrossRef]
32. Аль-Набхани, З.; Дюлаурой, С.; Маркес, Р.; Кусу, К.; Эл Банни, С.; Дежарден, Ф.; Спарвассер, Т.; Берард, М.; Серф-Бенсуссан, Н.; Эберл, Г. Для устойчивости к иммунопатологиям у взрослых необходимо снижение реакции на микробиоту. Иммунитет 2019, 50, 1276–1288. [Перекрестная ссылка] [PubMed]
33. Рубо-Бодрон, К.; Руис, В.Е.; Свон, А. М. младший; Валланс, бакалавр; Озкул, К.; Пей, З.; Ли, Дж.; Батталья, ТВ; Перес-Перес, Дж.И.; Блазер, М.Дж. Долгосрочное влияние воздействия антибиотиков в раннем возрасте на устойчивость к последующей бактериальной инфекции. мБио 2019, 10, е02820-19. [Перекрестная ссылка] [PubMed]
34. Кахенцли Дж.; Коллер, Ю.; Висс, М.; Геукинг, МБ; Маккой, К.Д. Кишечное микробное разнообразие во время колонизации в раннем возрасте формирует долгосрочные уровни IgE. Клетка-хозяин Microbe 2013, 14, 559–570. [Перекрестная ссылка] [PubMed]
35. Эль Айди, С.; Хойвелд, Г.; Тремароли, В.; Бэкхед, Ф.; Клееребезем, М. Микробиота кишечника и гомеостаз слизистой оболочки: колонизация при рождении или во взрослом возрасте, имеет ли это значение? Кишечные микробы 2013, 4, 118–124. [Перекрестная ссылка]
36. Ван, К.; Ли, К.; Рен, Дж. Взаимодействие микробиоты и иммунитета в патогенезе кишечной инфекции. Передний. Иммунол. 2019, 10, 1873. [CrossRef]
37. МакГакин, Массачусетс; Линден, СК; Саттон, П.; Флорин, Т.Х. Динамика муцинов и кишечные возбудители. Нат. Преподобный Микробиол. 2011, 9, 265–278. [Перекрестная ссылка]
38. Могенсен, Т.Х. Распознавание патогенов и передача воспалительных сигналов во врожденной иммунной защите. Клин. Микробиол. Ред. 2009, 22, 240–273. [Перекрестная ссылка]
9. Минарриета, Л.; Горбани, П.; Спарвассер, Т.; Берод, Л. Метаболиты: расшифровка молекулярного языка между DC и их средой. Семин. Иммунопатол. 2017, 39, 177–198. [Перекрестная ссылка]
40. Леви, М.; Колодзейчик, А.А.; Таисс, Калифорния; Элинав Э. Дисбиоз и иммунная система. Нат. Преподобный Иммунол. 2017, 17, 219–232. [Перекрестная ссылка]
41. Морикава, М.; Цуджибе, С.; Киёсима-Сибата, Дж.; Ватанабэ, Ю.; Като-Нагаока, Н.; Шида, К.; Мацумото, С. Микробиота тонкого кишечника избирательно поглощается фагоцитами собственной пластинки и пейеровых 0 бляшек. PLoS ONE 2016, 11, e0163607. [Перекрестная ссылка]
42. Колер А.; Дельбаув, С.; Смаут, Дж.; Торрес, Д.; Фламанд, В. Воздействие TNF, индуцированного микробиотой, в очень раннем возрасте приводит к созреванию неонатального pre-cDC1. Гут 2021, 70, 511–521. [Перекрестная ссылка] [PubMed]
43. Йоханссон, Мэн; Ханссон Г.К. Иммунологические аспекты кишечной слизи и муцинов. Нат. Преподобный Иммунол. 2016, 16, 639–649. [Перекрестная ссылка] [PubMed]
44. Хумаюн, М.; Аюсо, Дж. М.; Парк, Кентукки; Марторелли Ди Дженова, Б.; Скала, MC; Керр, Южная Каролина; Нолл, LJ; Биб, Д. Д. Реакция врожденных иммунных клеток на взаимодействие хозяина и паразита в микрофизиологической системе тканей кишечника человека. наук. Адв. 2022, 8, eabm8012. [Перекрестная ссылка] [PubMed]
45. Артис, Д.; Спитс, Х. Биология врожденных лимфоидных клеток. Природа 2015, 517, 293–301. [Перекрестная ссылка] [PubMed]
46. Ланкельма, Дж. М.; ван Вугт, Луизиана; Белзер, К.; Шульц, MJ; ван дер Полл, Т.; де Вос, WM; Виерсинга, В.Дж. Пациенты в критическом состоянии демонстрируют большие межличностные различия в нарушении регуляции кишечной микробиоты: пилотное исследование. Мед. интенсивной терапии. 2017, 43, 59–68. [Перекрестная ссылка]
47. Фурнье, Б.М.; Паркос, Калифорния. Роль нейтрофилов при воспалении кишечника. Мукозальный иммунол. 2012, 5, 354–366. [Перекрестная ссылка]
48. Лох, Дж. Т.; Ли, КГ; Ли, АП; Тео, JKH; Лим, Х.Л.; Ким, СС; Тан, А.Х.; Lam, KP. DOK3 поддерживает гомеостаз кишечника путем подавления передачи сигналов JAK2/STAT3 и продукции S100a8/9 в нейтрофилах. Смерть клетки Дис. 2021, 12, 1054. [CrossRef]
49. Со, Д.Х.; Че, Х.; Ким, С.; Ким, Д.Х.; Ма, Х.В.; Ким, Дж. Х.; Ким, ТИ; Ким, Вашингтон; Ким, Юго-Запад; Чеон, Дж. Х. Триггерный рецептор, экспрессируемый на миелоидных клетках, агонист -1 регулирует воспаление кишечника посредством нейтрофилов Cd177(+). Передний. Иммунол. 2021, 12, 650864. [CrossRef]
50. Вонг, Л.; Юнг, CW; Пиннелл, LJ; Шерман, П.М. Адгезивно-инвазивная Escherichia coli усугубляет вызванный антибиотиками кишечный дисбиоз и активацию внеклеточных ловушек нейтрофилов. Воспаление. Дис. кишечника. 2016, 22, 42–54. [Перекрестная ссылка]
51. Делано, МЮ; Уорд, Пенсильвания Роль иммунной системы в прогрессировании, разрешении и долгосрочном исходе сепсиса. Иммунол. Ред. 2016, 274, 330–353. [Перекрестная ссылка]
52. Апостолов А.К.; Хамани, М.; Эрнандес-Варгас, Х.; Игалузен, Р.; Гайеннон, А.; Фесно, О.; Мари, Джей Си; Судья, С.М. Общие и исключительные особенности кишечных интраэпителиальных гаммадельта-Т-клеток и других подмножеств гамма-дельта-Т-клеток. Иммуногоризонты 2022, 6, 515–527. [Перекрестная ссылка] [PubMed]
53. Исмаил А.С.; Северсон, КМ; Вайшнав, С.; Берендт, CL; Ю, Х.; Бенджамин, Дж.Л.; Рун, Калифорния; Хоу, Б.; ДеФранко, Алабама; Яровинский Ф.; и другие. Гаммадельта-интраэпителиальные лимфоциты являются важными медиаторами микробного гомеостаза хозяина на поверхности слизистой оболочки кишечника. Учеб. Натл. акад. наук. США 2011, 108, 8743–8748. [Перекрестная ссылка]
54. Холтмайер, В.; Кабелиц, Д. Гаммадельта Т-клетки связывают врожденные и адаптивные иммунные реакции. хим. Иммунол. Аллергия 2005, 86, 151–183. [Перекрестная ссылка]
55. Тайлер, СиДжей; Маккарти, штат Невада; Линдси, Дж.О.; Стэгг, Эй Джей; Мозер, Б.; Эберл, М. Антигенпрезентирующие гаммадельта Т-клетки человека способствуют экспрессии IL -22 Т-клетками CD4(+) кишечника и высвобождению кальпротектина в слизистой оболочке. Дж. Иммунол. 2017, 198, 3417–3425. [Перекрестная ссылка] [PubMed]
56. Ли, Ю.; Ван, Ю.; Ши, Ф.; Чжан, X.; Чжан, Ю.; Би, К.; Чен, X.; Ли, Л.; Диао, Х. Фосфолипидные метаболиты микробиоты кишечника способствуют повреждению кишечника, вызванному гипоксией, через CD1d-зависимые гамма-дельта Т-клетки. Кишечные микробы 2022, 14, 2096994. [CrossRef] [PubMed]
57. Томаселло, Э.; Бедуи, С. Клетки врожденного иммунитета кишечника в гомеостазе кишечника и иммунонадзоре. Иммунол. Клеточная Биол. 2013, 91, 201–203. [Перекрестная ссылка] [PubMed]
58. Гримальди, Д.; Ле Бури, Л.; Сонеф, Б.; Дешартр, А.; Руссо, К.; Уааз, Ф.; Милдер, М.; Луи, Д.; Чиче, доктор медицинских наук; Мира, Япония; и другие. Специфическое поведение клеток MAIT среди врожденных Т-лимфоцитов у пациентов в критическом состоянии с тяжелыми инфекциями. Мед. интенсивной терапии. 2014, 40, 192–201. [Перекрестная ссылка]
59. Андреу-Баллестер, JC; Тормо-Каландин, К.; Гарсия-Баллестерос, К.; Перес-Грьера, Дж.; Амиго, В.; Алмела-Куилис, А.; Руис дель Кастильо, судья; Пенарроха-Отеро, К.; Баллестер, Ф. Ассоциация гамма-дельта Т-клеток с тяжестью заболевания и смертностью у пациентов с сепсисом. Клин. Вакцина Иммунол. 2013, 20, 738–746. [Перекрестная ссылка]
60. Благородный, А.; Принг, ET; Дюрант, Л.; Мэн, Р.; Дилке, С.М.; Хойлс, Л.; Джеймс, ЮАР; Кардинг, СР; Дженкинс, Джей Ти; Найт, С.К. Изменение иммунитета к микробиоте, активация В-клеток и истощение гамма-дельта/резидентных Т-клеток памяти при колоректальном раке. Рак Иммунол. Иммунотер. 2022, 71, 2619–2629. [Перекрестная ссылка]
61. Сузуки, Х.; Чон, Ки; Ито, К.; Дой, К. Региональные различия в распределении интраэпителиальных лимфоцитов тонкой кишки у мышей, свободных от микробов и специфических патогенов. Эксп. Мол. Патол. 2002, 72, 230–235. [Перекрестная ссылка]
62. Бедуи, С.; Хит, WR; Мюллер, SN CD4(+) Т-клетки помогают усиливать врожденные сигналы первичного CD8(+) Т-клеточного иммунитета. Иммунол. Ред. 2016, 272, 52–64. [Перекрестная ссылка] [PubMed]
63. Белз, Г.Т.; Шортман, К.; Беван, MJ; Heath, WR CD8alpha+ дендритные клетки селективно представляют нецитолитические вирусные и внутриклеточные бактериальные антигены, ограниченные MHC класса I, in vivo. Дж. Иммунол. 2005, 175, 196–200. [Перекрестная ссылка] [PubMed]
64. Штейн, М.Б.; Баффорд, AC; Салерно-Гонсалвес, Воздействие серовара R. Salmonella enterica Typhi вызывает ex vivo эпигенетические изменения, специфичные для определенного типа клеток, в клетках кишечника человека. наук. Отчет 2020, 10, 13581. [CrossRef]
65. Бекаттини, С.; Литтманн, ER; Сок, Р.; Аморетти, Л.; Фонтана, Э.; Райт, Р.; Гьонбалай, М.; Лейнер, И.М.; Плитас, Г.; Холь, ТМ; и другие. Повышение иммунитета слизистой оболочки за счет временного истощения микробиоты. Нат. Коммун. 2020, 11, 4475. [CrossRef]
66. Де Вит, Дж.; Сауэр, Ю.; Йорритсма, Т.; Клаасс Бос, Х.; тен Бринке, А.; Нифджес, Дж.; ван Хэм, С.М. Антигенспецифические В-клетки реактивируют эффективный цитотоксический Т-клеточный ответ против фагоцитированной сальмонеллы посредством перекрестной презентации. PLoS ONE 2010, 5, e13016. [Перекрестная ссылка] [PubMed]
67. Шнелл, А.; Хуанг, Л.; Сингер, М.; Сингараджу, А.; Барилла, РМ; Риган, БМЛ; Болхаген, А.; Такоре, ИП; Дионн, Д.; Делори, ТМ; и другие. Стволоподобные кишечные клетки Th17 дают начало патогенным эффекторным Т-клеткам во время аутоиммунитета. Ячейка 2021, 184, 6281–6298.e23. [Перекрестная ссылка]
68. Оменетти, С.; Бюсси, К.; Метиджи, А.; Исеппон, А.; Ли, С.; Толайни, М.; Ли, Ю.; Келли, Г.; Чакраварти, П.; Шоаи, С.; и другие. Кишечник содержит функционально различные гомеостатические тканерезидентные и воспалительные клетки Th17. Иммунитет 2019, 51, 77–89. [CrossRef] 69. Иванов И.И.; Атараши, К.; Манель, Н.; Броди, Эл.; Шима, Т.; Караоз, У.; Вэй, Д.; Гольдфарб, КЦ; Санти, Калифорния; Линч, СВ; и другие. Индукция кишечных клеток Th17 сегментированными нитчатыми бактериями. Cell 2009, 139, 485–498. [Перекрестная ссылка]
70. Тан, Т.Г.; Сефик, Э.; Гева-Заторский Н.; Куа, Л.; Наскар, Д.; Тенг, Ф.; Пасман, Л.; Ортис-Лопес, А.; Джапп, Р.; Ву, HJ; и другие. Идентификация видов бактерий-симбионтов из кишечника человека, которые сами по себе могут индуцировать кишечные клетки Th17 у мышей. Учеб. Натл. акад. наук. США 2016, 113, E8141–E8150. [Перекрестная ссылка]
71. Сано, Т.; Кагеяма, Т.; Фанг, В.; Кедми, Р.; Мартинес, CS; Талбот, Дж.; Чен, А.; Кабрера, И.; Горшко О.; Куракаке, Р.; и другие. Избыточная потребность в цитокинах для дифференцировки клеток Th17, индуцированной кишечной микробиотой, в дренирующих лимфатических узлах. Cell Rep. 2021, 36, 109608. [CrossRef]
72. Айронс, Э.Э.; Кортес Гомес, Э.; Андерсен, В.Л.; Лау, JTY Бактериальная колонизация и иммунитет TH17 формируются кишечным сиалированием у новорожденных мышей. Гликобиология 2022, 32, 414–428. [Перекрестная ссылка] [PubMed]
73. Александр, М.; Анг, QY; Наяк, Р.Р.; Бустион, А.Е.; Сэнди, М.; Чжан, Б.; Упадхьяй, В.; Поллард, Канзас; Линч, СВ; Тернбо, П.Дж. Бактериальный метаболизм кишечника человека приводит к активации Th17 и колиту. Клетка-хозяин Microbe 2022, 30, 17–30. [Перекрестная ссылка] [PubMed]
74. Бреннан, Калифорния; Клэй, СЛ; Лавуа, СЛ; Бэ, С.; Ланг, Дж. К.; Фонсека-Перейра, Д.; Росинский, КГ; Оу, Н.; Гликман, Дж. Н.; Garrett, WS. Fusobacterium nucleatum управляет провоспалительным микроокружением кишечника посредством зависимой от метаболитных рецепторов модуляции экспрессии IL-17. Кишечные микробы 2021, 13, 1987780. [CrossRef] [PubMed]
75. Мальхов С.; Левенталь, Д.С.; Ли, В.; Ниши, С.; Соччи, Северная Дакота; Сэвидж, Пенсильвания. Айр усиливает иммунную толерантность, направляя аутореактивные Т-клетки в регуляторную линию Т-клеток. Иммунитет 2016, 44, 1102–1113. [Перекрестная ссылка]
76. Ян, С.; Фудзикадо, Н.; Колодин Д.; Бенуа, К.; Матис, Д. Иммунная толерантность. Регуляторные Т-клетки, образующиеся на ранних этапах жизни, играют особую роль в поддержании аутотолерантности. Наука 2015, 348, 589–594. [Перекрестная ссылка]
